Подробнее об эпидемиологии и возможных вариантах лечения пациентов с метастазами меланомы в головной мозг (ГМ) можно прочитать в статье. Внедрение в клиническую практику новых системных методов — таргетной терапии (ТТ), иммуноонкологической терапии (ИТ) и их комбинации — позволило значительно увеличить выживаемость данной когорты пациентов1,2. При этом в целом на лечение лучше реагируют пациенты с бессимптомными метастазами меланомы в ГМ2. В данной статье мы обсудим особенности применения ТТ, ИТ и их комбинации именно у этой группы пациентов. А узнать последние новости о лечении пациентов с симптомными метастазами можно здесь.
Основные исследования ТТ, ИТ и их комбинации у пациентов с бессимптомными метастазами меланомы кожи в ГМ
Клинические исследования эффективности ТТ и ИТ у пациентов с меланомой кожи проводятся более 20 лет. Однако в большинство исследований не были включены пациенты с метастазами в ГМ, поскольку метастатическое поражение ГМ связано с неблагоприятным прогнозом, и оценка эффективности лечения у таких пациентов должна проводиться отдельно1.
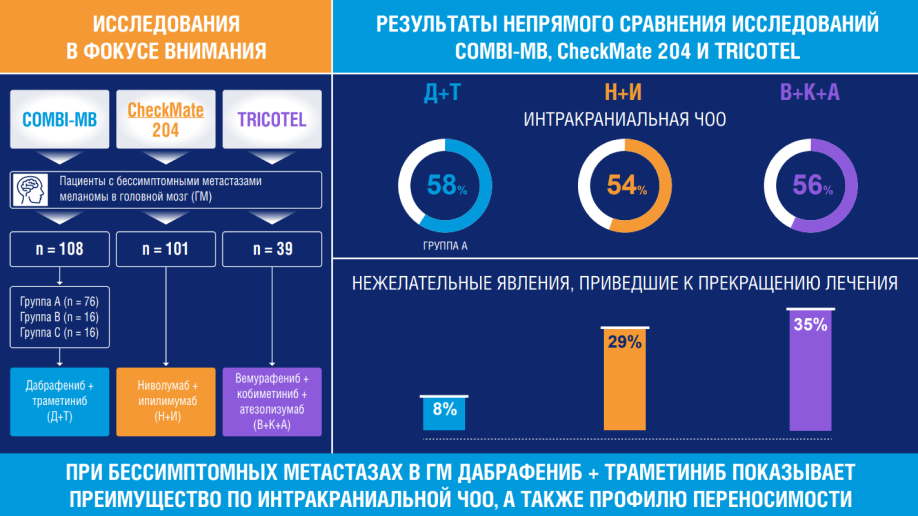
Мы обсудим три основных исследования ТТ, ИТ и их комбинации у пациентов с бессимптомными метастазами меланомы кожи в ГМ, которые включали когорты бессимптомных пациентов и показали достаточную эффективность: COMBI-MB, CheckMate 204 и TRICOTEL1,2,3,4.
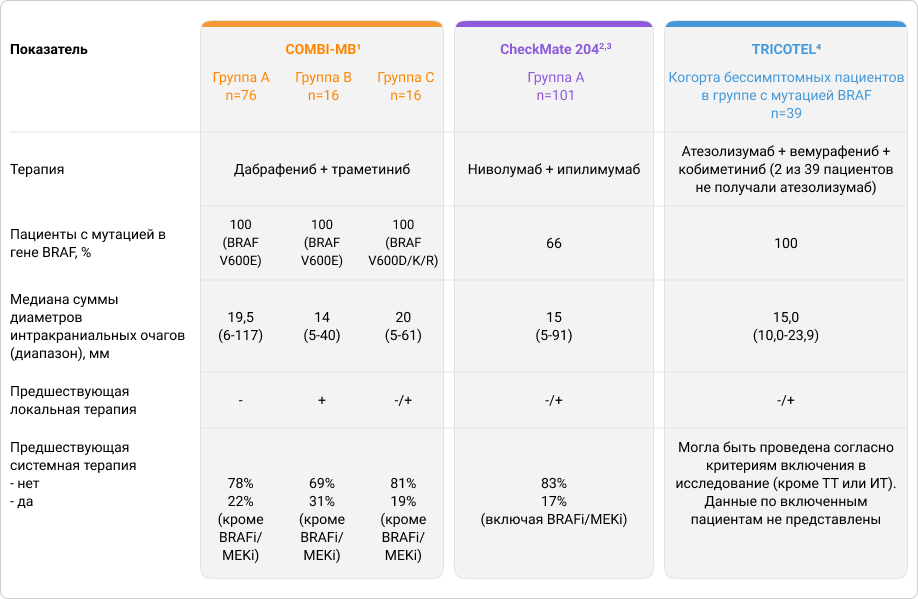
Таблица 1. Характеристика пациентов с бессимптомными метастазами меланомы кожи в ГМ в исследованиях COMBI-MB, CheckMate 204 и TRICOTEL
В исследовании COMBI-MB оценивали эффективность ТТ комбинацией дабрафениб + траметиниб у 3 групп пациентов (n=108) с бессимптомными метастазами меланомы кожи в ГМ с разными вариантами мутации BRAF V600, получавших или нет предшествующее местное лечение. В когортах, включающих пациентов, которые ранее получали местную терапию (группы В и С), предыдущие методы лечения могли включать трепанацию черепа, лучевую терапию всего ГМ и стереотаксическую радиохирургию. Во все группы могли быть включены пациенты, получавшие ранее до двух линий системной терапий, за исключением BRAFi/MEKi1.
В исследование CheckMate 204 были включены пациенты (n=101) с бессимптомными метастазами меланомы кожи в ГМ, которые получали ИТ комбинацией анти-PD1 и анти-CTLA4. Часть пациентов получала в качестве предшествующего лечения системную терапию (включая ТТ) и/или стереотаксическую радиохирургию2,3.
Эффективность комбинации ТТ+ИТ с применением триплета атезолизумаб + вемурафениб + кобиметиниб у пациентов с бессимптомными метастазами меланомы кожи в головной мозг оценивали в исследовании TRICOTEL (n=39). В исследование могли быть включены пациенты, получавшие предшествующую системную терапию (кроме ТТ и ИТ) и/или стереотаксическую радиохирургию4.
Непрямое сравнение эффективности ТТ, ИТ и их комбинации у пациентов с бессимптомными метастазами меланомы кожи в ГМ
Несмотря на то, что ни в одном исследовании у пациентов с бессимптомными метастазами меланомы кожи в ГМ напрямую не сравнивали эффективность ТТ, ИТ и их комбинации, можно провести их непрямое сравнение.
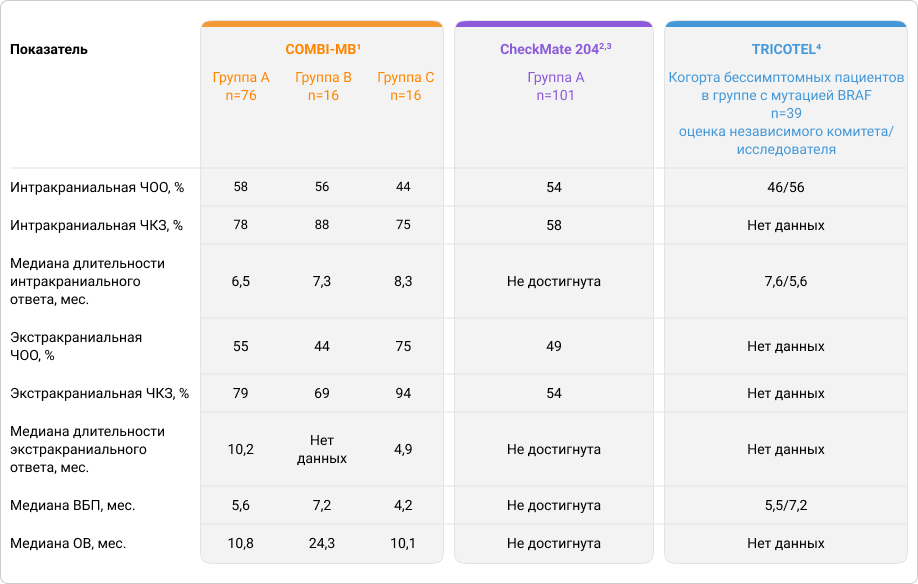
Таблица 2. Эффективность ТТ, ИТ и их комбинации у пациентов с бессимптомными метастазами меланомы кожи в ГМ в исследованиях COMBI-MB, CheckMate 204 и TRICOTEL
В исследовании COMBI-MB во всех группах пациентов с бессимптомными метастазами меланомы кожи в головной мозг был зарегистрирован ответ интракраниальных и экстракраниальных метастатических очагов меланомы (ЧОО от 44% до 75%; ЧКЗ от 69% до 94%). Медиана продолжительности интракраниального ответа составила 6,5–8,3 месяца в разных группах, экстракраниального ответа — 4,9–10,2 месяца1.
В исследовании CheckMate 204 в группе бессимптомных пациентов интракраниальные ЧОО и ЧКЗ составили 54% и 58% и были выше, чем соответствующие показатели для экстракраниальных очагов (49% и 54% соответственно). Медианы ВБП и ОВ у пациентов с бессимптомными метастазами в ГМ не были достигнуты при медиане наблюдения 20,6 месяцев2.
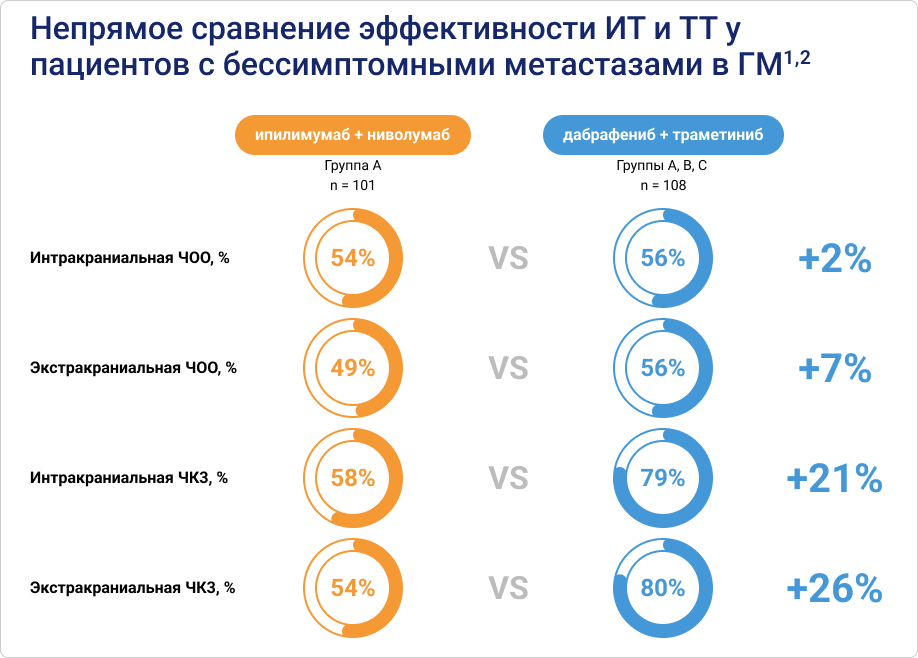
Нами было проведено непрямое сравнение результатов исследований CheckMate 204 и COMBI-MB в отношении пациентов с бессимптомными метастазами меланомы в ГМ.
По показателям ЧОО и ЧКЗ (как для интракраниальных, так и для экстракраниальных очагов) ТТ (суммарные данные по трем группам, включавшим бессимптомных пациентов) продемонстрировала большую эффективность, чем ИТ. Разница составляла от 2% до 26%1,2.
Провести сравнение результатов исследования COMBI-MB с результатами исследования TRICOTEL немного сложнее. Дело в том, что в исследовании TRICOTEL основной анализ результатов проводили целиком по группе пациентов с мутацией в гене BRAF, без выделения когорт симптомных и бессимптомных пациентов. Авторами представлены только отдельные данные по некоторым показателям у пациентов с бессимптомными метастазами меланомы кожи в ГМ, и в целом они соответствуют результатам применения комбинации дабрафениб + траметиниб в исследовании COMBI-MB: так, интракраниальная ЧОО для триплета составила 46% (по данным независимого комитета) и 56% (по данным исследователя) против 44–58% для комбинации дабрафениб + траметиниб1,4.
Влияние приема ГКС на эффективность терапии бессимптомных метастазов меланомы кожи в ГМ
По мнению исследователей, прием ГКС у пациентов с метастазами меланомы в ГМ может снизить выживаемость онкологических пациентов и эффективность ИТ2,5. Это влияние особенно важно для пациентов с симптомными метастазами, которые часто получают терапию ГКС. Узнать подробнее о результатах влияния приема ГКС на эффективность лечения данной когорты пациентов можно здесь. Однако для пациентов с бессимптомными метастазами, которые проходят лечение ИТ, вероятность приема ГКС в связи с развитием иммуноопосредованных НЯ (иоНЯ) также значительно возрастает. Согласно данным некоторых исследований, почти у половины пациентов на фоне ИТ развиваются иоНЯ, требующие приема ГКС6.
В исследовании CheckMate 204 в группу А были включены пациенты с бессимптомными метастазами меланомы в ГМ, не принимающие ГКС2. Принимая во внимание высокую вероятность развития у этих пациентов в реальной клинической практике НЯ, требующих приема ГКС6, можно ожидать что эффективность ИТ у пациентов с бессимптомными метастазами меланомы в ГМ может оказаться ниже, чем в самом исследовании CheckMate 204.
Безопасность различных вариантов системного лечения пациентов с метастазами меланомы в головной мозг
Переносимость комбинации дабрафениб + траметиниб1 у пациентов с бессимптомными метастазами меланомы кожи была значительно лучше, чем комбинации ипилимумаб + ниволумаб2,3 и триплета атезолизумаб + вемурафениб + кобиметиниб4.
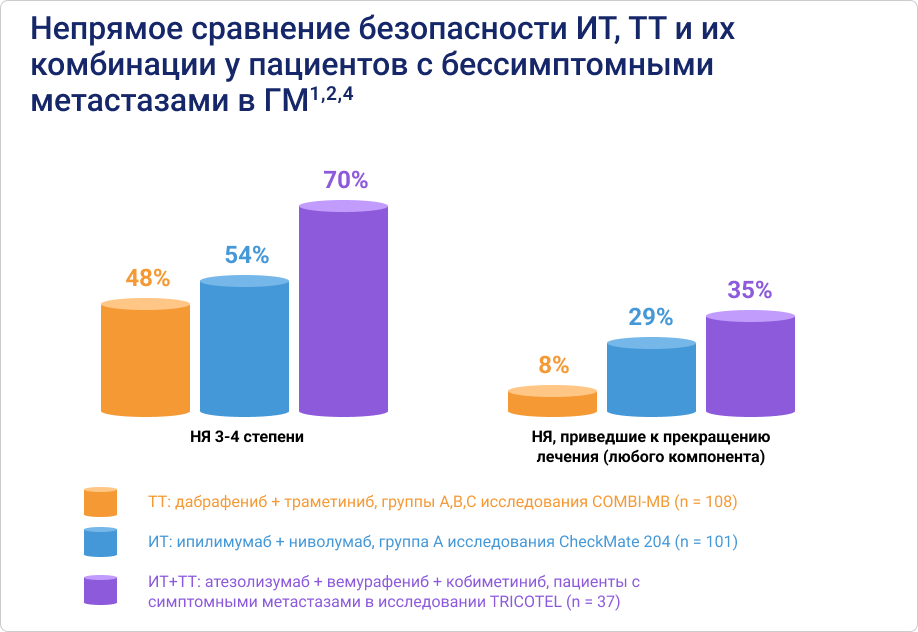
На фоне ИТ и ИТ+ТТ чаще развивались нежелательные явления (НЯ) 3-4 степени (на 6-22% чаще, чем для ТТ)1,2,4.
Пациенты, получавшие ИТ и ИТ+ТТ, прекращали лечение из-за развившихся НЯ примернов 4 раза чаще, чем при лечении ТТ1,2,4.
Кроме того, в исследовании CheckMate 204 была зарегистрирована одна смерть от миокардита, связанная с проводимым лечением2. При применении комбинаций дабрафениб + траметиниб и атезолизумаб + вемурафениб + кобиметиниб смертельных исходов, связанных с лечением, не было1.
Ключевые выводы
- В арсенале врача на сегодняшний день имеется три эффективные опции системного лечения пациентов с бессимптомными метастазами меланомы кожи в ГМ: ТТ, ИТ и их комбинация1,2,3,4.
- При применении комбинации дабрафениб + траметиниб показатели ЧОО и ЧКЗ (как для интракраниальных, так и для экстракраниальных очагов) были на 2–26% выше, чем при применении комбинации ипилимумаб + ниволумаб1,2.
- Добавление иммунного компонента к ТТ не привело к значительному повышению эффективности. В клинических исследованиях эффективность комбинации дабрафениба и траметиниба и триплета вемурафениба + кобиметиниба и атезолизумаба сопоставимы1,4:
- интракраниальная ЧОО 44-58% vs 46/56%;
- медиана длительности интракраниального ответа 6,5–8,3 месяцев vs 7,6/5,6 месяцев.
- Комбинация дабрафениб + траметиниб имеет более благоприятный профиль безопасности по сравнениюс ИТ и ИТ+ТТ1,2,4:
- В 4 раза ниже прекращение терапии из-за развития НЯ;
- На 6-22% реже развивались НЯ 3-4 степени.
Таким образом, комбинация дабрафениба и траметиниба обладает оптимальным соотношением эффективности и безопасности. При этом лучшие результаты (медиана ОВ — 24,3 месяца) были получены при применении ТТ вместе с локальной терапией (группа В в исследовании COMBI-MB)1,2,3,4.
Сокращения
BRAFi — ингибиторы BRAF
MEKi — ингибиторы МЕК
ВБП — выживаемость без прогрессирования
ГКС — глюкокортикостероиды
ГМ — головной мозг
ИТ — иммуноонкологическая терапия
иоНЯ — иммуноопосредованные нежелательные явления
НЯ — нежелательные явления
ОВ — общая выживаемость
ТТ — таргетная терапия
ЧКЗ — частота контроля заболевания
ЧОО — частота объективного ответа
Список литературы
- Davies M. A. et al. Dabrafenib plus trametinib in patients with BRAFV600-mutant melanoma brain metastases (COMBI-MB): a multicentre, multicohort, open-label, phase 2 trial //The Lancet Oncology. – 2017. – Т. 18. – №. 7. – С. 863-873.
- Tawbi H. A. et al. Safety and efficacy of the combination of nivolumab plus ipilimumab in patients with melanoma and asymptomatic or symptomatic brain metastases (CheckMate 204) //Neuro-oncology. – 2021. – Т. 23. – №. 11. – С. 1961-1973.
- Tawbi H. A. et al. Long-term outcomes of patients with active melanoma brain metastases treated with combination nivolumab plus ipilimumab (CheckMate 204): final results of an open-label, multicentre, phase 2 study //The lancet oncology. – 2021. – Т. 22. – №. 12. – С. 1692-1704
- Dummer R. et al. Atezolizumab, vemurafenib, and cobimetinib in patients with melanoma with CNS metastases (TRICOTEL): a multicentre, open-label, single-arm, phase 2 study // The Lancet Oncology. – 2023. – Т. 24. – №. 14. – С. 1470-2035.
- Long G. V. et al. Combination nivolumab and ipilimumab or nivolumab alone in melanoma brain metastases: a multicentre randomised phase 2 study //The Lancet Oncology. – 2018. – Т. 19. – №. 5. – С. 672-681.
- O’Reilly A. et al. An immunotherapy survivor population: health-related quality of life and toxicity in patients with metastatic melanoma treated with immune checkpoint inhibitors //Supportive Care in Cancer. – 2020. – Т. 28. – С. 561-570.
11338318/ONCO/DIG/12.24/0