Многих онкологов волнует вопрос: если пациенту с меланомой кожи проводили таргетную терапию (ТТ), а потом по каким-то причинам она была прекращена (прогрессирование, развитие побочных эффектов, недоступность препарата), может ли дать клинический эффект повторное назначение ТТ?
В большинстве случаев возврат к ТТ оправдан и показывает хорошую эффективность у пациентов с меланомой кожи, у которых ранее был получен клинический ответ на ТТ. Это касается даже тех пациентов, у которых при первом назначении ТТ после улучшения наступало прогресирование1, 2 .
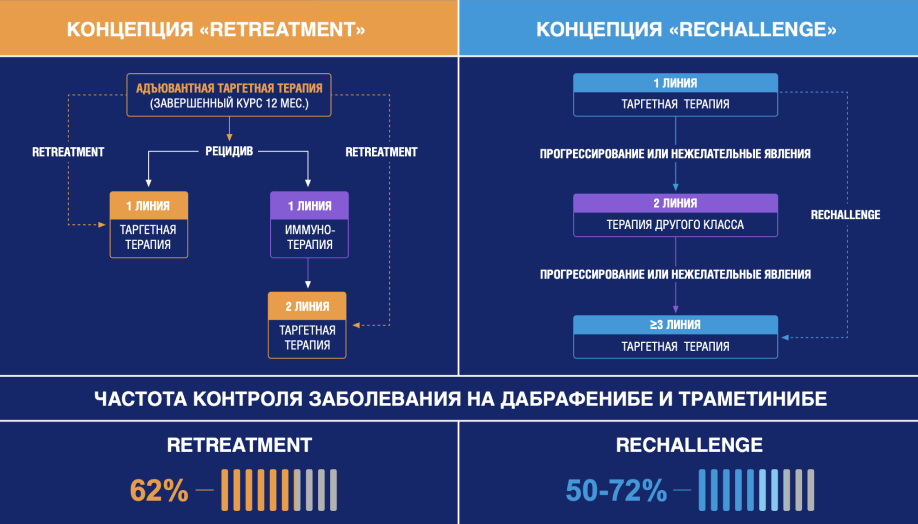
Понятия retreatment и rechallenge
Существуют два близких понятия, описывающих возврат к ТТ: retreatment и rechallenge1 .
Retreatment
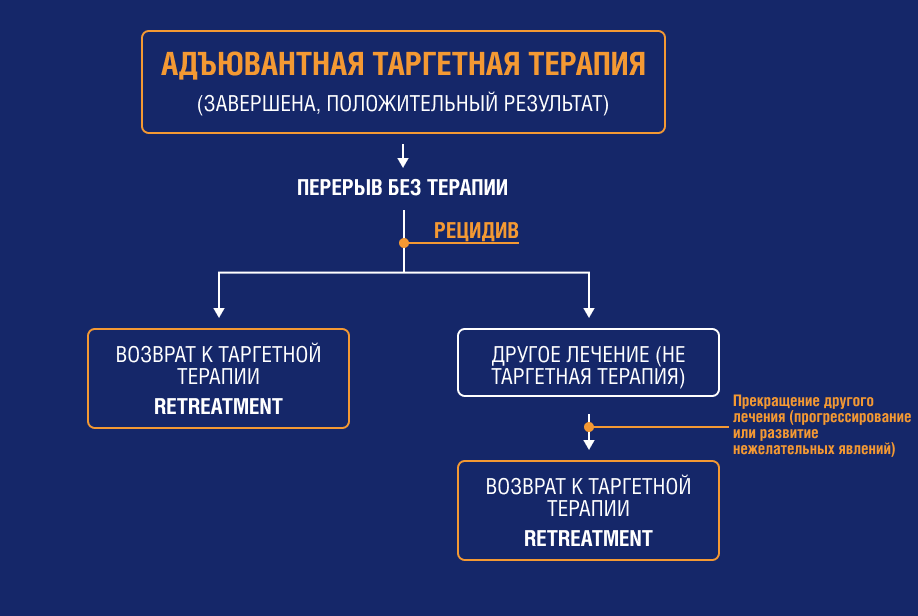
Если пациент с меланомой кожи завершил полный курс адъювантной ТТ с положительным результатом, затем был перерыв без лекарственной терапии, после чего возник рецидив, то в этом случае возврат к ТТ описывается термином retreatment1 .
Retreatment может быть проведен не сразу после рецидива, а как терапия второй линии, если сразу после рецидива пациенту был назначен другой метод лечения, но лечение было прервано из-за прогрессирования или развития нежелательных явлений1 .
Rechallenge
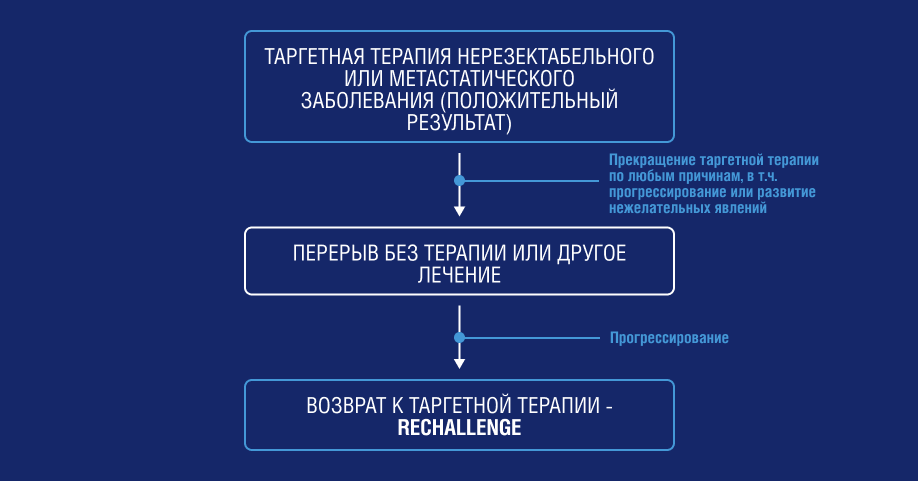
Пациентам с нерезектабельной или метастатической меланомой кожи может быть назначена повторная ТТ после прерывания лечения по разным причинам. В этом случае возврат к ТТ обозначается термином rechallenge1 .
Молекулярные механизмы, обеспечивающие эффективность возврата к ТТ
Retreatment
После успешной адъювантной ТТ отдельные опухолевые клетки могут выжить и остаться в организме. С течением времени из них снова может развиться меланома. Эта рецидивная опухоль может быть чувствительна к ТТ, потому что развилась она из клеток чувствительного клона1 .
Rechallenge
Сложнее объяснить эффективность возврата к ТТ у пациентов с метастатической меланомой, особенно если отказ от первой линии ТТ произошел по причине прогрессирования опухолевого процесса на фоне ТТ после первоначального улучшения. Однако клинические данные подтверждают эффективность возврата к ТТ и в данном случае1,2 . Исследователи объясняют это следующим образом.
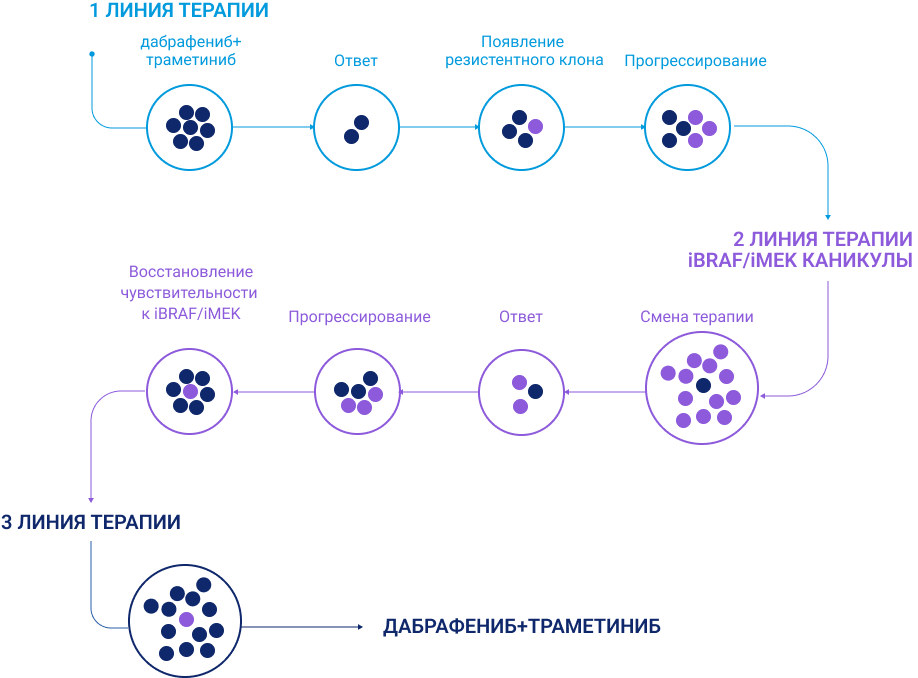
Появление резистентных к ТТ клонов опухолевых клеток может также происходить в процессе лечения1. Применение ТТ вызывает регрессию чувствительных клонов клеток, при этом резистентные к действию ТТ клоны выживают1.
Однако в результате лечения популяция чувствительных к ТТ клеток может быть уничтожена не полностью. При прогрессировании опухоли после второй линии терапии (не ТТ) рост опухоли может быть связан как раз с увеличением популяции чувствительных к ТТ опухолевых клеток. В этом случае опухоль вновь будет отвечать на ТТ1.
Итак, основной механизм, обеспечивающий эффективность возврата к ТТ, – восстановление с течением времени популяции чувствительных к ТТ опухолевых клеток. Но есть и второй механизм – обратимая резистентность. Некоторые приобретенные механизмы резистентности (например, реактивация пути МАРК выше BRAF – активация RAS, или ниже BRAF – активация MEK1 или МЕК2) могут быть обратимыми после прекращения ТТ, и спустя время опухоль может восстановить чувствительность к ТТ1.
Клинические подтверждения эффективности возврата к ТТ
Ряд исследований и отдельных наблюдений подтверждают эффективность возврата к ТТ у пациентов с меланомой кожи, у которых ранее был получен клинический ответ на ТТ.
Rechallenge
В 2019 году был опубликован большой обзор, в котором были представлены результаты повторного применения ТТ ингибиторами BRAF и MEK суммарно у 238 пациентов с метастатической меланомой кожи2. Интервал между первым и повторным применением ТТ составлял не менее 4 недель. В целом было показано, что пациенты реагировали на повторное применение препаратов, даже если у них ранее наблюдалось прогрессирование заболевания на фоне ТТ. ЧОО в среднем составила 47%, ЧКЗ – 67%. Медиана ВБП составляла от 4,9 до 11 месяцев в разных сериях наблюдений.
На ASCO 2023 было сообщено о результатах повторного лечения по поводу первого прогрессирования метастатической меланомы у 26 пациентов. В данной группе ЧОО составила 38,5%, ЧКЗ — 50%, медиана ВБП — 11,1 месяцев, медиана ОВ — 22,2 месяца3.
Важно отметить, что длительность эффекта после повторного лечения, как правило, меньше чем после начальной терапии1.
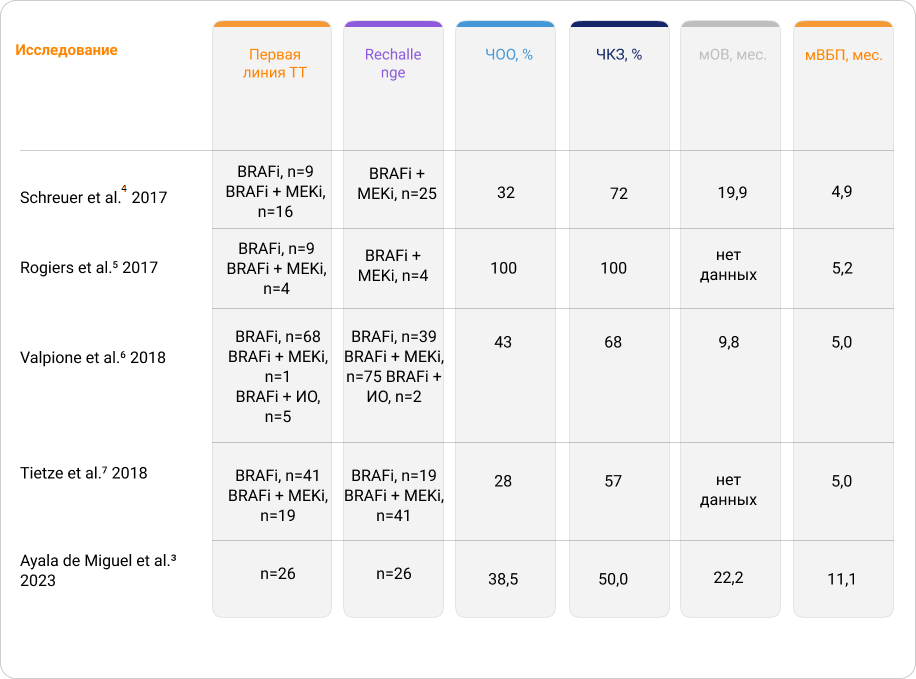
Таблица – Результаты основных исследований клинической эффективности возврата к ТТ у пациентов с метастатической/прогрессирующей меланомой кожи
В целом эффективность возврата к таргетной терапии у пациентов с метастатической или прогрессирующей меланомой можно оценить, как достаточно высокую, учитывая, что это терапия третьей и последующих линий, и состояние пациентов более тяжелое, чем в начале лечения. При этом показатели эффективности в некоторых исследованиях (Schreuer et al.4, медиана ОВ — 19,9 месяцев; Ayala de Miguel et al.3, медиана ОВ — 22,2) сопоставимы с эффективностью первой линии ТТ в более ранних исследованиях, например в исследовании COMBI–d/v8 (медиана ОВ — 25,9 месяца).
Retreatment
Данных по эффективности возврата к адъювантной ТТ у пациентов с меланомой кожи существенно меньше.
На ASCO 2020 были представлены результаты возврата к ТТ у 13 пациентов с рецидивом меланомы кожи после адъювантной ТТ: ЧОО составила 46,2%, ЧКЗ — 61,5%9. На ASCO 2023 было сообщено о 4 пациентах, которые получали повторную ТТ по поводу рецидива меланомы после адъювантной ТТ. Срок от окончания адъювантной ТТ до повторной ТТ составил в среднем 17,8 месяцев. ЧОО у данных пациентов составила 25%, медиана ВБП – 5,7 месяцев, медиана ОВ – 8,5 месяцев3.
Является ли возврат к ИТ таким же эффективным, как возврат к ТТ?
Учитывая высокую эффективность возврата к ТТ у пациентов с меланомой кожи, возникает резонный вопрос, будет ли возврат к ИТ демонстрировать такие же хорошие результаты.
Исследования показывают, что возврат к ИТ оправдан только у пациентов, прекративших ИТ первой линии по причине развившейся токсичности. Возврат к ИТ после отмены из-за прогрессирования заболевания оказался менее эффективным10.
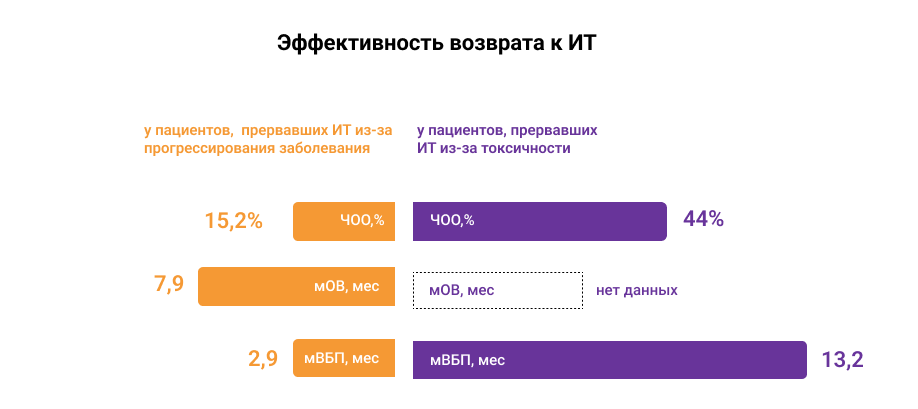
В 2021 году были опубликованы результаты мета-анализа эффективности возврата к ИТ по данным 49 исследований, в том числе по 24 – у пациентов с меланомой кожи (n = 4380)10. У пациентов (со всеми нозологиями), прекративших первое лечение ИТ в связи с прогрессированием, ЧОО составила всего 15,2%, медиана ВБП — 2,9 месяца, медиана ОВ — 7,9 месяца. У пациентов, прекративших первое лечение ИТ по причине развившейся токсичности, показатели эффективности повторной ИТ были выше: ЧОО — 44%, медиана ВБП — 13,2 месяца10.
Рисунок – Эффективность возврата к ИТ у пациентов, прервавших лечение из-за токсичности терапии или прогрессирования заболевания (все нозологии)10
Таким образом, возврат к ИТ может быть оправдан, но только у пациентов, прервавших ранее лечение ИТ из-за развившихся НЯ10.
Ключевые выводы
В большинстве случаев возврат к ТТ оправдан и показывает хорошую эффективность у пациентов с меланомой кожи, у которых ранее был получен клинический ответ на ТТ2,3.
Стратегия повторного применения ТТ после перерыва в лечении у пациентов с меланомой кожи основана на возможности1:
- восстановления популяции чувствительных к BRAFi/MEKi клеток в период перерыва в лечении после первой линии ТТ;
- обратимости механизмов приобретенной вторичной резистентности к ТТ.
Даже если ранее наблюдалось прогрессирование заболевания на фоне ТТ, пациенты, как правило, реагировали на повторное применение BRAFi/MEKi2.
У пациентов с метастатической меланомой при возврате к ТТ ЧКЗ в среднем составляла 65%, медиана ВБП — от 4,9 до 11,1 месяцев и медиана ОВ — от 9,8 и 22,2 месяцев в разных сериях наблюдений2,3.
Список сокращений
ВБП — выживаемость без прогрессирования
иоНЯ — иммуноопосредованные нежелательные явления
ИТ — иммунотерапия
мОВ — медиана общей выживаемости
мВБП — медиана выживаемости без прогрессирования
НЯ — нежелательные явления
ОВ — общая выживаемость
ТТ — таргетная терапия
ЧКЗ — частота контроля заболевания
ЧОО — частота объективного ответа
Источники
- Gebhardt C. et al. The concepts of rechallenge and retreatment in melanoma: a proposal for consensus definitions //European Journal of Cancer. – 2020. – Т. 138. – С. 68–76.
- Reschke R., Simon J. C., Ziemer M. Rechallenge of targeted therapy in metastatic melanoma //JDDG: Journal der Deutschen Dermatologischen Gesellschaft. – 2019. – Т. 17. – №. 5. – С. 483–486.
- Ayala de Miguel P. et al. Retreatment and rechallenge with BRAF/MEK inhibitors in patients with metastatic melanoma: Results from the observational study GEM1801 (ASCO 2023). – 2023. – С. 9547.
- Schreuer M. et al. Combination of dabrafenib plus trametinib for BRAF and MEK inhibitor pretreated patients with advanced BRAFV600–mutant melanoma: an open–label, single arm, dual–centre, phase 2 clinical trial //The Lancet Oncology. – 2017. – Т. 18. – №. 4. – С. 464–472.
- Rogiers A., Wolter P., Bechter O. Dabrafenib plus trametinib rechallenge in four melanoma patients who previously progressed on this combination //Melanoma research. – 2017. – Т. 27. – №. 2. – С. 164–167.
- Valpione S. et al. Rechallenge with BRAF–directed treatment in metastatic melanoma: A multi–institutional retrospective study //European Journal of Cancer. – 2018. – Т. 91. – С. 116–124.
- Tietze J. K. et al. The efficacy of re–challenge with BRAF inhibitors after previous progression to BRAF inhibitors in melanoma: A retrospective multicenter study //Oncotarget. – 2018. – Т. 9. – №. 76. – С. 34336.
- Robert C. et al. Five–year outcomes with dabrafenib plus trametinib in metastatic melanoma //New England Journal of Medicine. – 2019. – Т. 381. – №. 7. – С. 626–636.
- Bhave P. et al. Melanoma recurrence after adjuvant targeted therapy: A multicenter analysis (ASCO 2023) //Journal of Clinical Oncology. – 2020. – Т. 38. – № 15. – С. 10016.
- Inno A. et al. Rechallenge of immune checkpoint inhibitors: A systematic review and meta–analysis //Critical Reviews in Oncology/Hematology. – 2021. – Т. 165. – С. 103434
11338317/ONCO/DIG/12.24/0