Кости являются третьим наиболее частым местом метастазирования для широкого спектра солидных опухолей, включая:
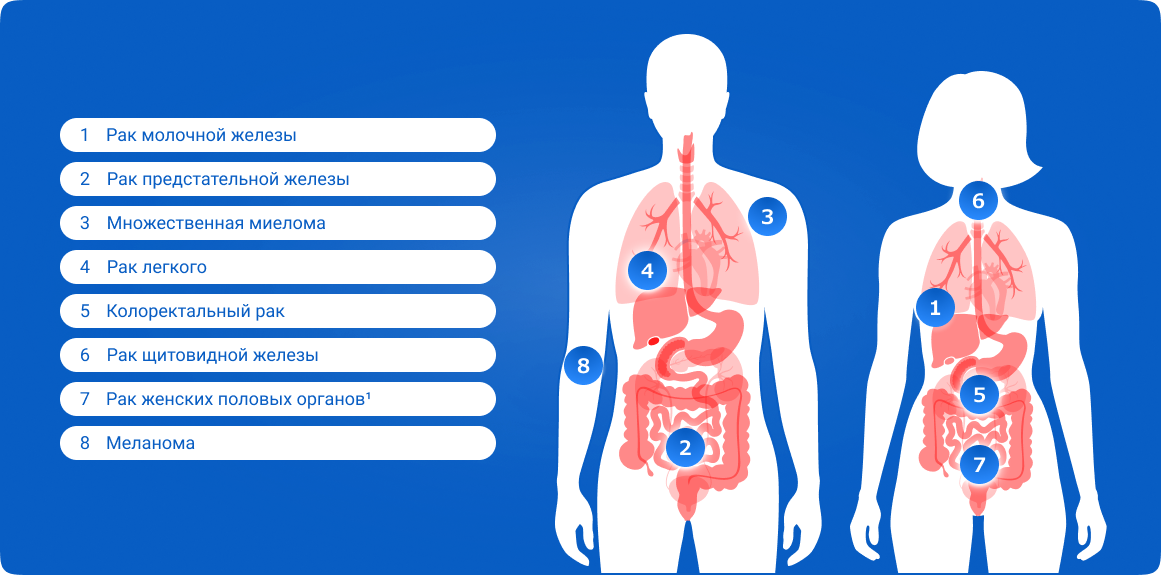
Частота метастатического поражения скелета при раке молочной железы (РМЖ) составляет по разным данным 65–75%.2,3 В одном из исследований на вскрытиях установлено, что у 90,1% мужчин, умерших от гематогенныхметастазов рака предстательной железы, были диагностированы костные метастазы.4
В наше время трудно представить лечение этих опухолей без добавления остеомодифицирующих агентов в связи с тем, чтоосложнения метастазов в кости (так называемые «скелетные события») – переломы, компрессия спинного мозга, болевойсиндром - сильно снижают качество жизни пациентов.5-8
Цель применения антирезорбтивной лекарственной терапии – купирование болевого синдрома, предотвращение или отсрочкаскелетных событий. Сохраняя плотность костной ткани, обеспечивается качество жизни пациента: мобильность, снижается необходимость в постороннем уходе.9,10
Механизм действия
По своей химической структуре бисфосфонаты (БФ) являются аналогами пирофосфатов костного матрикса. БФ связываются с кальцием, накапливаются в костях, утилизируются зрелыми остеокластами, угнетая их активность. Золедроновая кислота оказывает на них прямое апоптотическое действие. In vivo: ингибирует резорбцию костной ткани остеокластами, изменяет микросреду костного мозга, приводит к снижению темпа роста опухолевых клеток; проявляет антиангиогенную активность.11-13,27
Золедроновая кислота, благодаря синергическому эффекту в комбинации с гормональной терапией или химиотерапией подавляет пролиферацию и индуцирует апоптоз, оказывает непосредственное противоопухолевое действие в отношении клеток миеломы человека и рака молочной железы.27

У пациентов с раком молочной железы, раком предстательной железы и другими солидными опухолями с метастатическим поражением костей золедроновая кислота предотвращает развитие патологических переломов, компрессии спинного мозга, снижает потребность в проведении лучевой терапии и оперативных вмешательств, уменьшает опухолевую гиперкальциемию.
Препарат способен сдерживать прогрессирование болевого синдрома.27
У пациентов с опухолевой гиперкальциемией действие препарата характеризуется снижением содержания кальция в сыворотке крови и выведения кальция почками. Среднее время до нормализации содержания кальция составляет около 4 дней.27
Помимо антирезорбтивного, золедроновая кислота может оказывать непосредственное противоопухолевое, антиангиогенное и иммуномодулирующее действие.1

Эффективность
Даже при отсутствии клинических проявлений метастазов в кости на ранних этапах их формирования всегда присутствует высокий риск костных осложнений.
Скелетные осложнения, в течение первых 2 лет, регистрируются в14-17:
При раке молочной железы
При раке простаты
Рак легкого и др.
Более 2 десятков рандомизированных исследований, в которых участвовали почти 11 тысяч пациенток, были посвящены изучению эффективности и безопасности остеомодифицирующих агентов (ОМА) при РМЖ с метастазами в кости. Польза ОМА при метастазах РМЖ в кости в отношении скелетных осложнений несомненна: это снижение их риска и частоты, увеличение времени до первого и последующих скелетных событий, а в некоторых исследованиях – улучшение результатов лечения в плане выживаемости (при нормализации маркеров костной резорбции).
Самым эффективным из БФ является золедроновая кислота, которая в ряде рандомизированных исследований продемонстрировала преимущество перед другими БФ в отношении скелетных осложнений.19
В рандомизированном исследовании фазы III по сравнению эффективности золедроновой кислоты и памидроната были включены в общей сложности 1130 пациенток, у которых были все типы костных метастазов по данным рентгенологического исследования (остеолитические, смешанные или остеобластные). Медиана времени до первого скелетного осложнения была значительно больше при лечении золедроновой кислотой в сравнении с памидронатом (310 и 174 дней соответственно, р=0,013). Кроме того, риск развития скелетных осложнений в группе золедроновой кислоты был ниже – на 20% для всехпациентов (р=0,037) и на 30% в подгруппе с остеолитическими очагами (р=0,010).20
Качество жизни
При этом в большинстве исследований при стратификации пациентов по уровню болевого синдрома (подгруппы с отсутствующим и легким болевым синдромом и с умеренным и выраженным) отмечается преимущество золедроновой кислоты над более ранними БФ.19 Медиана времени до начала использования наркотических анальгетиков в группе золедроновой кислоты составила 29,5 мес.21
Профиль безопасности
Наиболее частой нежелательной реакцией на золедроновую кислоту была гипофосфатемия.
анемия, головная боль, парестезии, конъюнктивит, тошнота, рвота, снижение аппетита, запор, повышенное потоотделение, нарушение сна, боль в костях, миалгия, артралгия, генерализованные боли, тугоподвижность суставов, повышение артериального давления, нарушение функции почек, повышение концентрации креатинина и мочевины в сыворотке крови, гипокальциемия, реакция острой фазы, повышение температуры тела, гриппоподобный синдром (включающий общее недомогание, озноб, чувство недомогания, «приливы»), периферические отеки, астения.27
Одна из нежелательных реакций, которые требуют особого внимания, – нефротоксичность. Частота этого нежелательного явления (НЯ) со стороны почек по данным клинических испытаний при разных злокачественных опухолях составила: множественная миелома (3,2%), рак простаты (3,1%), рак молочной железы (4,3%), рак легкого и другие солидные опухоли (3,2%).27 Также не менее важным осложнением терапии золедроновой кислотой является остеонекроз челюсти.Частота его возрастает с длительностью терапии и составляет от 1,2% до 6,2%. Совместное использование золедроновойкислоты с антиангиогенными препаратами, кортикостероидами резко повышает вероятность возникновения данногоосложнения.18,22,23
Влияние на профиль безопасности золедроновой кислоты можно добиться путем снижения интенсивности терапии без потери вэффективности.
В трех рандомизированных исследованиях сравнивали эффективность золедроновой кислоты, вводимой каждые 4 недели, всравнении с введением каждые 12 недель. В исследование ZOOM (NCT05361408) включались пациентки, которые ранееполучали ежемесячно золедроновую кислоту в течение 12–15 месяцев. Частота скелетных осложнений достоверно неотличалась в группе 12 недель по сравнению с ежемесячным введением. Наиболее частыми побочными явлениями 3–4 степенибыли боль в костях, тошнота и астения, нефротоксичность и остеонекроз челюсти развивались редко, без достоверныхразличий в зависимости от режима введения.24 В другом крупном рандомизированном открытом клиническомисследовании CALGB (NCT00869206), в которое были включены пациенты с метастатическим РМЖ, метастатическим ракомпредстательной железы и множественной миеломой, у одинакового количества пациентов (менее 30%) в группах 4-недельного и 12-недельного введения в течение 2 лет после рандомизации возникло как минимум одно скелетноеосложнение.
Таким образом, снижение интенсивности дозирования золедроновой кислоты не приводило к увеличению риска скелетныхосложнений течение 2 лет. Частота развития НЯ, в частности, остеонекроза челюсти и нарушения функции почек, были сопоставимы.26 В рандомизированное исследование OPTIMIZE-2 включались пациентки с РМЖ, которые ранееполучали золедроновую кислоту и/или памидронат в стандартном режиме. Через 1 год наблюдения скелетные осложнениявозникли у 22,0% пациентов в группе золедроновой кислоты каждые 4 недели и у 23,2% пациентов в группе золедроновойкислоты каждые 12 недель, и время до первого скелетного осложнения между группами лечения статистически значимо неразличалось. Профили безопасности в группах были сопоставимы.20,25
Ссылки:
- Understanding the Bone in Cancer Metastasis. Jaime Fornetti, Alana L Welm, Sheila A Stewart J Bone Miner Res 2018 Dec;33(12):2099-2113. doi: 10.1002/jbmr.3618. https://pubmed.ncbi.nlm.nih.gov/30476357/
- Faustine W, Stephen J, Aimee SJ. Geographical Location and Stage of Breast Cancer Diagnosis: A Systematic Review of the Literature. Journal of Health Care for the Poor and Underserved. 2016.
- Harvey HA. Issue concerning the role of chemotherapy and hormonal therapy of bone metastases from breast cancer.Cancer. 1997; 80(8): 1646-56.
- Bubendorf L., Schöpfer A., Wagner U., Sauter G., Moch H., Willi N., Gasser T.C., Mihatsch M.J. Metastatic patterns of prostate cancer: An autopsy study of 1,589 patients. Hum. Pathol. 2000;31:578–583. doi: 10.1053/hp.2000.6698
- Профилактика и лечение патологии костной ткани при злокачественных новообразованиях (rosoncoweb.ru) Практические рекомендации RUSSCO 2022 UJL
- Клинические рекомендации АОР https://oncology.ru/association/clinical-guidelines/
- NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines®) Breast Cancer Version 4.2023 breast.pdf (nccn.org)
- NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines®) Prostate Cancer. Version 1.2023 https://www.nccn.org/professionals/physician_gls/pdf/prostate.pdf
- Kennecke H, Yerushalmi R, Woods R, Cheang MCU, Voduc D, et al. Metastatic Behavior of Breast Cancer Subtypes. JCO. 2010; 28: 3271-3277.
- Gdowski et al. Journal of Experimental & Clinical Cancer Research. 2017; 36: 108
- D’Oronzo S, Coleman R, Brown J, Silvestris F. Metastatic bone disease:pathogenesis and therapeutic options: up-date on bone metastasis management. J Bone Oncol. 2019; 15: 004.
- Sousa S, Clézardin P. Bone-targeted therapies in cancer-induced bone disease. Calcif. Tissue Int. 2018; 102: 227-250.
- Roelofs AJ, Thompson K, Ebetino H, Rogers MJ, Coxon FP. Bisphosphonates: molecular mechanisms of action and effects on bone cells, monocytes and macrophages. Curr. Pharm. Des. 2010; 16: 2950–2960.
- Lipton A, Theriault RL, Hortobagyi GN, et al. Pamidronate prevents skeletal complications and is effective palliative treatment in women with breast carcinoma and osteolytic bone metastases: long term follow-up of two randomized, placebo-controlled trials. Cancer. 2000; 88: 1082-1090. Available at: http://www.ncbi.nlm.nih.gov/pubmed/10699899.
- Saad F, Gleason DM, Murray R, et al. Zoledronic acid is well tolerated for up to 24 months and significantly reduces skeletal complications in patients with advanced prostate cancer metastatic to bone. Am Urol Assoc. 2003; abstract 1472.
- Berenson JR, Lichtenstein A, Porter L, et al. Long-term pamidronate treatment of advanced multiple myeloma patients reduces skeletal events. Myeloma Aredia Study Group. J Clin Oncol. 1999; 16: 593-602.
- Coleman RE. Clinical features of metastatic bone disease and risk of skeletal morbidity. Clin Cancer Res. 2006; 12: 6243se6249s
- Багрова С.Г., Владимирова Л.Ю., Абрамова Н.А. 13.01.2023 Дискуссионная сцена. Бессимптомные метастазы в кости при раке молочной железы: лечить или наблюдать? (rosoncoweb.ru)
- O'Carrigan B, Wong MHF, Willson ML, Stockler MR, Pavlakis N, Goodwin A. Bisphosphonates and other bone agents for breast cancer. Cochrane Database of Systematic Reviews. 2017; Issue 10, Art. CD003474. DOI: 10.1002/14651858.CD003474.pub4.
- Stopeck AT, Lipton A, Body JJ, et al. Denosumab compared with zoledronic acid for the treatment of bone metastases in patients with advanced breast cancer: A randomized, double-blind study. J Clin Oncol. 2010; 28: 5132-5139. http://www.ncbi.nlm.nih.gov/pubmed/21060033
- Cleeland CS, Body J, Stopeck A, et al. Pain Outcomes in Patients With Advanced Breast Cancer and Bone Metastases. Cancer. 2013; 119: 832–8.
- Kozlow W, Guise TA. Breast Cancer Metastasis to Bone: Mechanisms of Osteolysis and Implications for Therapy. J Mammary Gland Biol Neoplasia. 2005; 10: 169-180.
- Von Moos R, Costa L, Gonzalez-Suarez E, et al. Management of bone health in solid tumours: from bisphosphonates to a monoclonal antibody. Cancer Treat Rev. 2019; 76: 57e67.
- Himelstein AL, Foster JC, Khatcheressian JL, et al. Effect of Longer-Interval vs Standard Dosing of Zoledronic Acid on Skeletal Events in Patients With Bone Metastases: A Randomized Clinical Trial. JAMA. 2017; 317: 48-58. Available at: https://www.ncbi.nlm.nih.gov/pubmed/28030702 A Clinical Trial to Evaluate Efficacy of Once or Twice ZOledronic Acid After Different Duration of denOsumMab Administration in Postmenopausal Women With Osteoporosis (ZOOM Study) - Full Text View - ClinicalTrials.gov
- Yang M, Yu X. Management of bone metastasis with intravenous bisphosphonates in breast cancer: a systematic review and meta-analysis of dosing frequency. Support Care Cancer. 2020; 28 (6): 2533e2540
- Zoledronic Acid in Treating Patients With Metastatic Breast Cancer, Metastatic Prostate Cancer, or Multiple Myeloma With Bone Involvement - Full Text View - ClinicalTrials.gov
- Инструкция по медицинскому применению препарата Зомета (золедроновая кислота). Препараты «Новартис Фарма» | Novartis Russia
451388/ZOM/WEB/052024/1

