
В настоящее время существенное значение для принятия решений о выборе терапии и оценки эффективности/безопасности лечения имеет анализ данных, полученных в условиях рутинной практики. Ранее эффективность комбинации BRAF-ингибитора дабрафениба и MEK-ингибитора траметиниба для лечения пациентов с метастатическим немелкоклеточным раком легкого (мНМРЛ) с мутацией BRAF V600E была показана в регистрационном клиническом исследовании II фазы [1].
Ниже вы найдете результаты исследования применения дабрафениба и траметиниба у пациентов с BRAF V600E мНМРЛ в реальной клинической практике, которые подтверждают и в некоторой мере превосходят результаты регистрационного исследования [2].
Дизайн исследования
IFCT-2004 BLaDE — многоцентровое ретроспективное когортное исследование с использованием вторичных данных, в котором изучались пациенты с мНМРЛ с мутацией BRAF V600E, получавшие комбинированную терапию дабрафенибом и траметинибом [2].
Отбор пациентов
В исследовании приняли участие 54 французских медицинских центра и 32 национальные диагностические лаборатории. Всего в исследование было включено 163 пациента, которым был поставлен диагноз «мНМРЛ с мутацией BRAF V600E» в период с 01.01.2016 по 31.12.2019 г. Пациенты получали комбинацию дабрафениба (D) и траметиниба (T) (D 300 мг + T 2 мг ежедневно) независимо от линии терапии [2].
Конечные точки исследования
Первичная конечная точка — 12-месячная общая выживаемость (ОВ) в группе пациентов, получавших D + T во 2-й и более поздних линиях.
Авторы также оценивали ОВ за 12-, 18- и 24-месячные периоды у пациентов, получавших комбинацию дабрафениба и траметиниба в 1 линии и 2+ линиях; выживаемость без прогрессирования (ВБП), частоту объективного ответа (ЧОО), профиль безопасности, а также эффективность последующей терапии [2].
Результаты
Характеристика популяции
Из 163 пациентов, включенных в исследование:
- 50,3% составили женщины;
- 30,2% пациентов никогда не курили;
- у 95,1% пациентов гистологический подтип — аденокарцинома;
- у 78,2% пациентов уровень экспрессии PD-L1 > 1%.
Медианный возраст составил 68,3 года.
На момент начала терапии D + T 80,8% пациентов имели ECOG 0/1 и у 93,9% пациентов была либо опухоль на IIIB/C стадии, не подлежащая хирургическому удалению, либо опухоль на IV стадии; у каждого пятого (20,9%) пациента были метастазы в головном мозге [2].
Эффективность терапии в зависимости от линии
Из 163 пациентов, принимавших участие в исследовании, 44 пациента (27%) получали D + T в 1 линии, а 119 пациентов (73%) — во 2+ линии.
На момент сбора данных (30.06.2021) медиана наблюдения составила 27,4 мес. (95% ДИ: 22,2–31,9) и 47 пациентов (28,8%) продолжали получать первоначальную терапию [2].
Первичная конечная точка — 12-месячная ОВ у пациентов, получавших комбинацию дабрафениба и траметиниба в 2+ линии, составила 67,4% (95% ДИ: 57,8–75,3) с мВБП — 10,4 мес. [2].
У 44 пациентов, получавших комбинацию дабрафениба и траметиниба в 1 линии, 12-месячная ОВ также составила 67% (95% ДИ: 51,2–79,3) с мВБП — 18,2 мес. [2].
Частота объективного ответа составила 82,9% (95% ДИ: 71,4–94,4) для пациентов, принимавших комбинацию дабрафениба и траметиниба в 1-ю линию, а для пациентов, получавших эту комбинацию во 2+ линию, ЧОО составила 73,8% (95% ДИ: 65,5–82,2).
После прогрессирования на комбинации дабрафениба с траметинибом 37,2% пациентов 2+ линии в качестве дальнейшего лечения получали иммунотерапию, 58,3% — химиотерапию. Для пациентов, получавших D + T в первой линии, последующая иммунотерапия назначалась в 42,9% случаев, химиотерапия — в 42,7% случаев.
мОВ пациентов, получавших комбинацию дабрафениба и траметиниба, составила 24,1 мес. (95% ДИ: 12,3–37,9) и 19,7 мес. (95% ДИ: 15,7–26,9) для 1 линии и 2+ линии соответственно, что согласуется с данными клинических исследований [2].
Непрямое сравнение результатов исследования РКП IFCT-2004 BLaDE и регистрационного клинического исследования II фазы NCT01336634
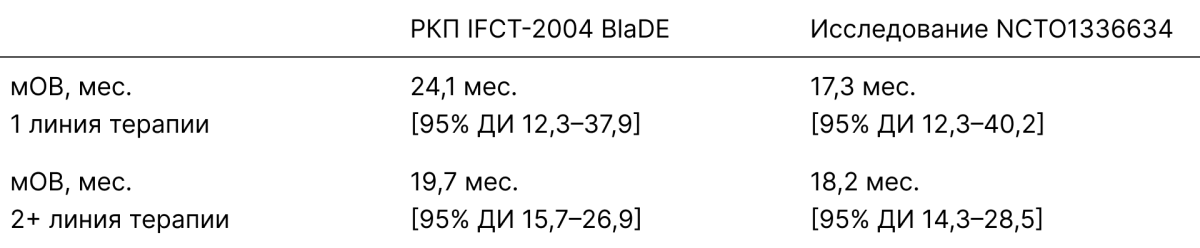
Примечание.
мВБП — медиана выживаемости без прогрессирования; ДИ — доверительный интервал; мОВ — медиана общей выживаемости; ЧОО — частота объективного ответа.
Безопасность
Всего 10,3% пациентов прекратили терапию дабрафенибом с траметинибом из-за нежелательных явлений, что согласуется с данными клинических исследований.
Самым частым нежелательным явлением при приеме препаратов дабрафениб и траметиниб является пирексия [1]. С новым алгоритмом управления пирексией, который позволяет снизить частоту тяжелых случаев, вы можете ознакомиться здесь.
Заключение
В рутинной практике эффективность дабрафениба и траметиниба у пациентов с BRAF V600E-мутированным мНМРЛ согласуется с данными, полученными в клинических исследованиях. Данные реальной клинической практики подтверждают эффективность использования дабрафениба и траметиниба не только во второй и последующих линиях, но также и в первой линии терапии. При этом частота объективного ответа, медиана ВБП и медиана ОВ выше при применении комбинации дабрафениба с траметинибом в 1 линии, чем при назначении во 2+ линиях [2].
Источники:
- Planchard et al. Phase 2 Study of Dabrafenib Plus Trametinib in Patients With BRAF V600E-Mutant Metastatic NSCLC: Updated 5-Year Survival Rates and Genomic Analysis. J Thorac Oncol. 2022;17:103-115.
- Swalduz A. et al. Efficacy of dabrafenib-trametinib combination in BRAF V600E-mutated metastatic non—small cell lung cancer: Results of the IFCT-2004 BLaDE cohort. J Clin Oncol. 2022;40:16 suppl, 9082-9082.
694139/ONCO/DIG/08.23/0

