Алпелисиб является ингибитором фосфатидилинозитол-3-киназы (PI3K), специфично подавляющим альфа-изоформу каталитической субъединицы данного фермента (PI3Kα)1. Селективная блокада именно альфа-изоформы обеспечивает высокую эффективность и приемлемый профиль переносимости терапии2. Основные нежелательные явления, возникающие на фоне приема алпелисиба (гипергликемия и сыпь), напрямую связаны с механизмом действия препарата, поскольку PI3K не только стимулирует деление клеток, но и участвует в регуляции уровня глюкозы в крови и дифференцировки клеток кожи (эпидермиса)3,4.
Гипергликемия, диарея и сыпь — это основные предсказуемые и управляемые нежелательные явления, которые отмечаются на фоне терапии алпелисибом. По данным исследования SOLAR-1, гипергликемия, диарея и сыпь любой степени интенсивности отмечались у 64%, 58% и 36% пациентов соответственно, а 3–4 степень интенсивности отмечалась у 36%, 10% и 7% пациентов.
Спектр НЯ, зарегистрированных в популяции исследования SOLAR-1, представлен в табл. 15.
Таблица 1 — Наиболее частые НЯ, возникавшие на фоне терапии алпелисибом или плацебо в исследовании SOLAR-1
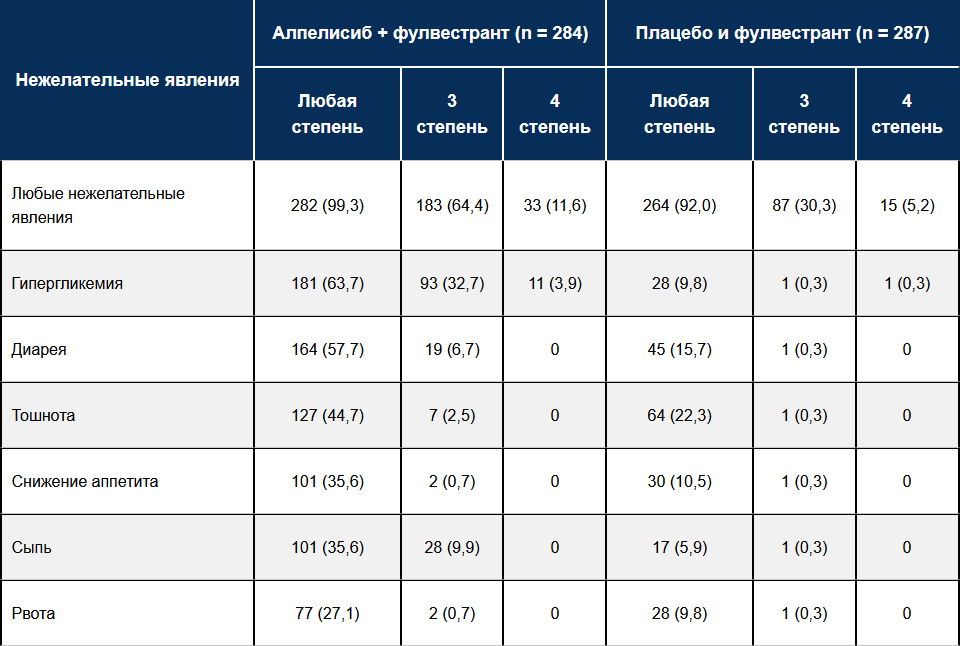
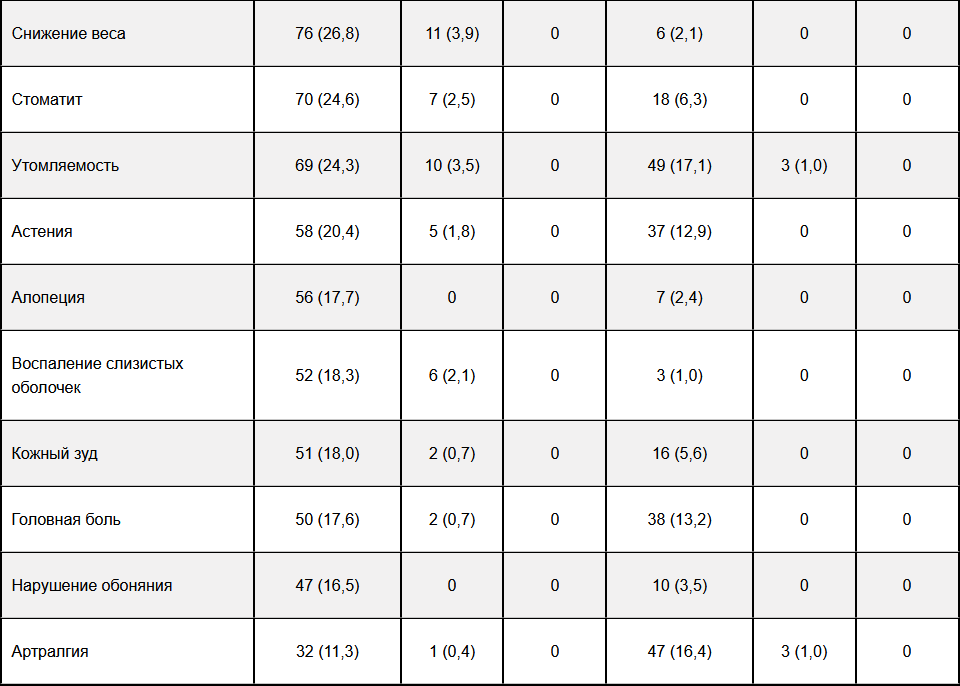
Сроки развития и разрешения основных НЯ при приеме алпелисиба по данным исследования SOLAR-1 представлены в табл. 2.
Таблица 2 — Время развития и разрешения целевых НЯ на фоне терапии алпелисибом
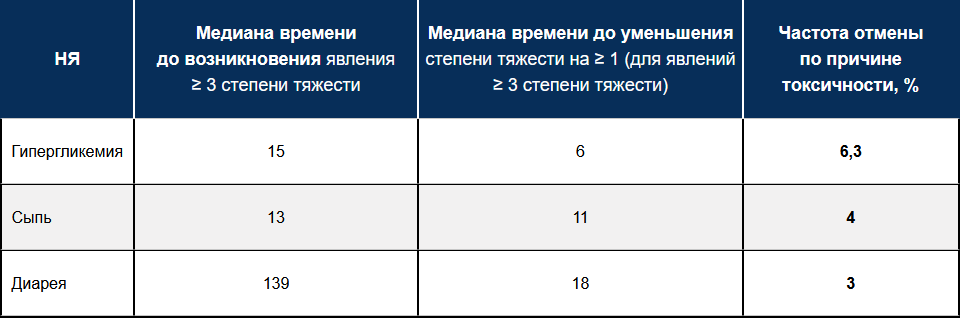
По данным исследования SOLAR-1, временный перерыв в приеме препарата по причине развития НЯ потребовался 69% пациентов, коррекция дозы — 62% пациентов и 25% пациентов вынуждены были прекратить терапию алпелисибом и фулвестрантом из-за НЯ2. Гипергликемия являлась причиной прекращения терапии алпелисибом у 6,3% пациентов, сыпь — у 3,2%, диарея — у 2,8% пациентов.
Для НЯ 3 и 4 степени интенсивности предусмотрено снижение дозы алпелисиба сначала до 250 мг, а затем при необходимости до 200 мг в сутки (табл. 3).
Таблица 3 — Схема редукции дозы алпелисиба
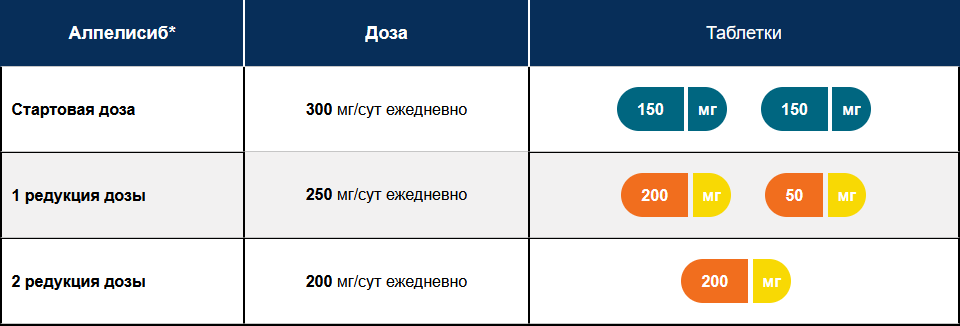
Для большинства НЯ:
-
Прервать прием до восстановления или до ≤ 1 степени тяжести.
-
Снизить дозу при повторном развитии соответствующего НЯ.
Медиана интенсивности дозы алпелисиба составила 248 мг/день (83,7%). Показатели выживаемости без прогрессирования при применении высоких доз алпелисиба были выше, чем при назначении низких доз препарата, однако более высокая эффективность по сравнению с плацебо отмечалась при применении обоих режимов (рис. 1)5.
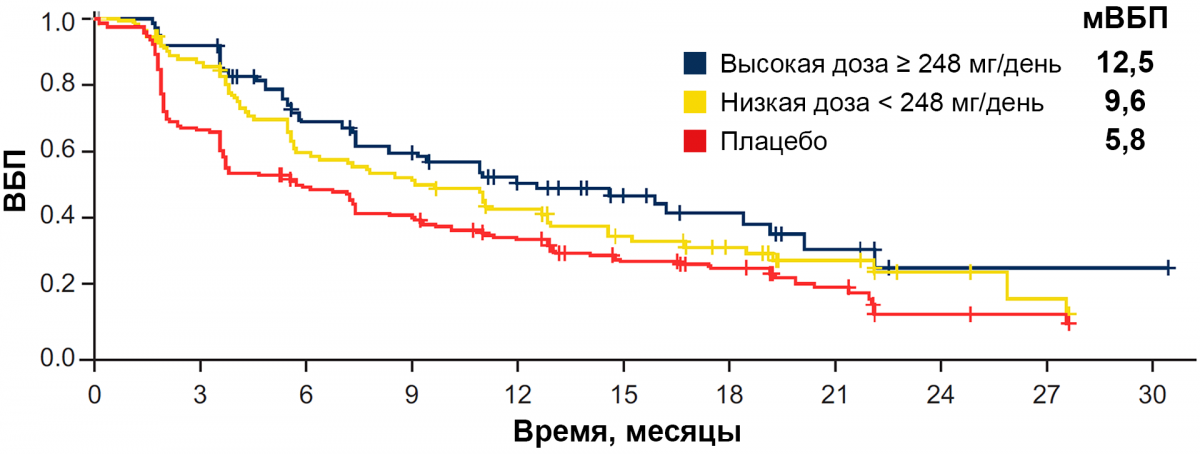
Примечание.
ВБП — выживаемость без прогрессирования; мВБП — медиана выживаемости без прогрессирования (мес.).
Рисунок 1 — Снижение дозы алпелисиба и эффективность терапии
Список источников:
- Fritsche C., Huang A., Chatenay-Rivauday C. et al. Characterization of the novel and specific PI3Ka inhibitor NVP-BYL719 and development of the patient stratification strategy for clinical trials. Mol Cancer Ther. 2014;13:1117e1129.
- André F., Ciruelos E., Rubovszky G. et al. Alpelisib for PIK3CA-Mutated, Hormone Receptor-Positive Advanced Breast Cancer. N Engl J Med. 2019;380(20):1929-1940. doi:10.1056/NEJMoa1813904.
- Świderska E. et al. DOI:10.5772/intechopen.80402.
- Calautti E., Li J., Saoncella S. et al. Phosphoinositide 3-kinase signaling to Akt promotes keratinocyte differentiation versus death. J Biol Chem 2005; 280(38): 32856–32865.
- Rugo H.S., Andre F., Yamashita T. et al. Time course and management of key adverse events during the randomized phase III SOLAR-1 study of PI3K inhibitor alpelisib plus fulvestrant in patients with HR-positive advanced breast cancer. Annals of Oncology. Volume 31, Issue 8, August 2020, Pages 1001-1010.
790570/WEB/GEN/04.24/1
