Алпелисиб — таргетный препарат, который применяют в комбинации с фулвестрантом для лечения пациентов с гормонозависимым HER2-отрицательным распространенным раком молочной железы (HR+ HER2- рРМЖ) с мутациями гена PIK3CA и резистентностью к эндокринной терапии (ЭТ) [1–3]. Алпелисиб можно назначать как в 1-й, так и в последующих линиях терапии, но в реальной клинической практике этот препарат используют, как правило, после ингибиторов CDK4/6 [2–6]. Эффективность алпелисиба у таких пациентов изучали в многоцентровом открытом исследовании II фазы BYLieve* [7]. В когорте А исследования BYLieve пациенты (n = 121) получали алпелисиб с фулвестрантом после прогрессирования на фоне терапии ингибитором CDK4/6 в комбинации с летрозолом. Медиана ВБП составила 7,3 мес. (95% ДИ 5,6–8,3) [7], что оказалось в два раза больше, чем мВБП при других вариантах терапии**, используемых в реальной клинической практике (3,6 мес.; 95% ДИ: 3,1–6,1) [8]. Новый анализ данных исследования BYLieve, представленный на конгрессе SABCS 2022, демонстрирует, что длительного контроля заболевания (ВБП ≥ 12 мес.) удалось достичь каждой четвертой пациентке (25,6%, 31/121), причем из них 16,5% (20/121) достигли очень длительного контроля (≥ 18 мес.) [9]. В подгруппе длительного (≥ 12 мес.) ответа медиана ВБП составила 24,8 мес. (95% ДИ: 18,2–НД), в подгруппе очень длительного (≥ 18 мес.) ответа — 29,4 мес. (95% ДИ: 24,8–33,1). В подгруппе пациенток с ВБП < 12 мес. медиана ВБП составила 5,4 мес. (95% ДИ: 3,7–5,8) (рис. 1).
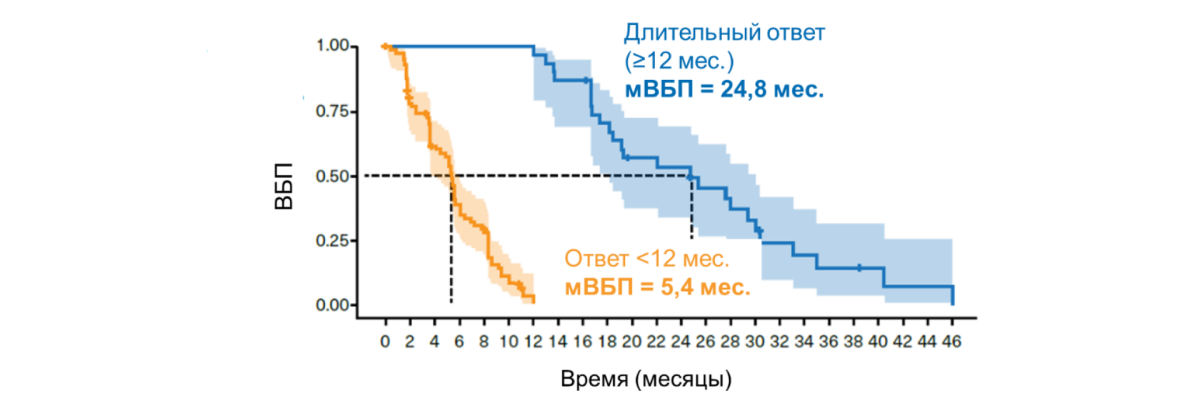
Рисунок 1. ВБП в подгруппах пациентов с ВБП ≥ 12 мес. и < 12 мес. (когорта А, исследование BYLieve) [9]
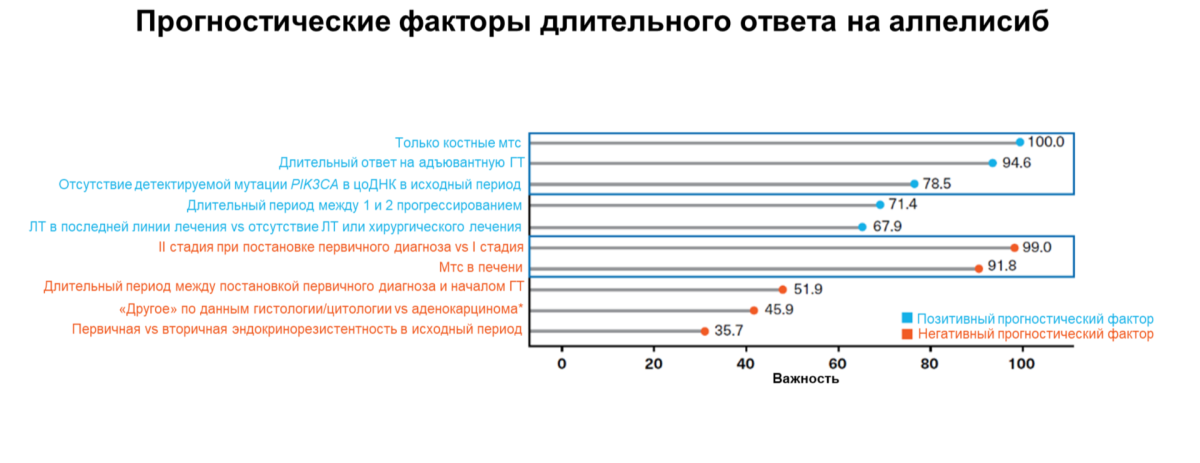
Основными предикторами длительного ответа на терапию алпелисибом являются костные метастазы, продолжительный ответ на адъювантную терапию, отсутствие детектируемой мутации PIK3CA в цоДНК в исходный период (рис. 2). При этом нежелательные явления (НЯ), в т. ч. диарея и гипергликемия, не коррелируют с развитием длительного ответа [9].
Примечания.
* «Другое» включает дольковую карциному in situ, недифференцированную карциному, «не применимо» и «другое». Мтс — метастазы; ГТ — гормонотерапия; цоДНК — циркулирующая опухолевая дезоксирибонуклеиновая кислота; ЛТ — лучевая терапия.
Рисунок 2. Прогностические факторы, ассоциированные с длительным ответом на терапию алпелисибом в когорте А исследования BYLieve [9]
Ранее в исследовании SOLAR-1*** было показано, что 30,2% пациентов смогли достичь длительного (ВБП > 18 мес.) контроля над заболеванием на фоне терапии алпелисибом с фулвестрантом. Большая часть этих пациентов (72,5%) достигли ВБП ≥ 24 мес. (до 49,7 мес.) [10]. Медиана ВБП в подгруппе пациентов с длительным контролем заболевания составила 33,5 мес. (95% ДИ: 27,4–НД) на фоне терапии алпелисибом с фулвестрантом и 25,6 мес. (95% ДИ: 22,1–29,7) на фоне терапии только фулвестрантом [10]. Факторами, ассоциированными с длительным ответом на терапию алпелисибом в исследовании SOLAR-1, были длительный безрецидивный период, малое количество очагов метастазирования, только костные метастазы, отсутствие метастазов в печень, низкий статус ECOG и чувствительность к ЭТ. Важно, что такие факторы, как неблагоприятный прогноз, наличие диабета/предиабета в исходный период, а также высокая степень предлеченности, не препятствовали достижению долгосрочного контроля заболевания [10]. Таким образом, анализ когорты А в исследовании BYLieve доказывает, что пациенты с HR+ HER2- рРМЖ с мутациями PIK3CA, получающие алпелисиб после прогрессирования на фоне терапии ингибитором CDK4/6, могут контролировать заболевание продолжительно — более 2 лет [9]. Поскольку НЯ не коррелируют с длительностью ответа, получить преимущество могут все пациенты, в том числе с риском развития гипергликемии в исходный период [9]. Эти результаты подтверждают и расширяют данные исследования SOLAR-1, полученные ранее [10].
Источники:
- Общая характеристика лекарственного препарата Пикрэй (алпелисиб) ЛП-№(000328)-(РГ-RU)-290721.
- Клинические рекомендации. Рак молочной железы. 2021. Электронный ресурс: https://cr.minzdrav.gov.ru/recomend/379_4 (Дата последнего обращения – 15.12.2022).
- Тюляндин С.А. с соавт. Практические рекомендации по лекарственному лечению рака молочной железы. Злокачественные опухоли: Практические рекомендации RUSSCO #3s2, 2021 (том 11). 09.
- NCCN Clinical Practice Guidelines in Oncology. Breast Cancer. Version 8.2021 – September 13, 2021. https://www.nccn.org/professionals/physician_gls/default.aspx (Дата последнего обращения – 15.12.2022).
- Gennari A. et al. ESMO Clinical Practice Guideline for the diagnosis, staging and treatment of patients with metastatic breast cancer. Annals of Oncology. 2021. 32(12):1475-1495.
- Burstein H.J. et al. Endocrine Treatment and Targeted Therapy for Hormone Receptor-Positive, Human Epidermal Growth Factor Receptor 2-Negative Metastatic Breast Cancer: ASCO Guideline Update. J Clin Oncol. 2021 Jul 29:JCO2101392.
- Rugo H. et al. Alpelisib (ALP) + fulvestrant (FUL) in patients (pts) with PIK3CA-mutated (mut) hormone receptor-positive (HR+), human epidermal growth factor receptor 2-negative (HER2–) advanced breast cancer (ABC) previously treated with cyclin-dependent kinase 4/6 inhibitor (CDKi) + aromatase inhibitor (AI): BYLieve study results. J Clin Oncol. 2020;38(15_suppl): abstr 1006. DOI: 10.1200/JCO.2020.38.15_suppl.1006
- Turner S. et al. 309P - Real-world effectiveness of alpelisib (ALP) + fulvestrant (FUL) compared with standard treatment among patients (Pts) with hormone-receptor positive (HR+) human epidermal growth factor receptor-2 negative (HER2–) PIK3CA-mutated (Mut) advanced breast cancer (ABC). Ann Oncol. 2020;31(suppl_4): S348-S395. DOI: 10.1016/annonc/annonc268
- Rugo H. et al. Long-Term and Very-Long-Term Disease Control in Patients from BYLieve Study Cohort A With PIK3CA-Mutant, Hormone Receptor-Positive, Human Epidermal Growth Factor Receptor 2-Negative, Advanced Breast Cancer. SABCS Dec 6-10, 2022. PD13-06.
- Juric D., Andre F., Panwar U. et al. Long-term (LT) disease control in patients (pts) with hormone receptor-positive (HR+), PIK3CA-altered advanced breast cancer (ABC) treated with alpelisib (ALP) + fulvestrant (FUL). J Clin Oncol 39, 2021 (suppl 15; abstr 1054).
* BYLieve — открытое многоцентровое несравнительное исследование алпелисиба II фазы, проводимое в трех когортах пациентов с гормонозависимым HER2- рРМЖ с мутацией PIK3CA, получавших ранее ингибитор CDK4/6 в комбинации с гормонотерапией. Когорта А (n = 121): пациенты, ранее получавшие ингибитор CDK4/6 с летрозолом, получали алпелисиб с фулвестрантом. Первичная конечная точка достигнута: через 6 мес. терапии 50,4% пациентов были живы без прогрессирования (95% ДИ 41,2–59,6). ** Химиотерапия, гормонотерапия, эверолимус (данные базы Flatiron Health, США), непрямое сравнение. *** SOLAR-1 — рандомизированное плацебо-контролируемое двойное слепое многоцентровое исследование III фазы для оценки эффективности и переносимости комбинации алпелисиба с фулвестрантом у пациентов с HR+ HER2- рРМЖ с мутацией PIK3CA, получавших ранее ЭТ (n = 572). Первичная конечная точка достигнута: мВБП составила 11,0 мес. в группе алпелисиба с фулвестрантом против 5,7 мес. в группе плацебо с фулвестрантом (ОР 0,65; 95%ДИ 0,50–0,85, p < 0,001).
Сокращения: ВБП — выживаемость без прогрессирования заболевания, ДИ — доверительный интервал, НД — не достигнуто, цоДНК — циркулирующая опухолевая ДНК.
778504/web/gen/03.24/1

