Патогенез
Чаще всего, но не всегда, в основе первичного миелофиброза (ПМФ) лежит молекулярная аномалия — драйверная мутация генов янус-киназы 2 (JAK2)1,2.
Основная функция янус-киназ заключается в передаче цитокинового сигнала в ядро клетки, который запускает ее пролиферацию посредством JAK-STAT сигнального пути2. При возникновении точечной мутации в нуклеотиде гена JAK2 происходит независимая активация фосфорилирования янус-тирозинкиназы даже при отсутствии стимуляции рецепторов. Это приводит к пролиферации клеток миелоидного ростка1,2.
Миелопролиферативные заболевания могут развиваться вследствие мутации тромбопоэтинового рецептора MPL или кальретикулина (CALR). Мутации CALR и JAK2 являются, как правило, взаимоисключающими. Мутация в гене тромбопоэтинового рецептора (MPL) вызывает усиленную пролиферацию мегакариоцитов. Клональная пролиферация сопровождается образованием экстрамедуллярных очагов кроветворения, большей частью в селезенке, и развитием фиброза костного мозга. Кроме того, медиаторы воспаления и цитокины, вырабатываемые трансформированным клоном и клетками костномозгового микроокружения, вызывают неспецифическую воспалительную реакцию1,2.
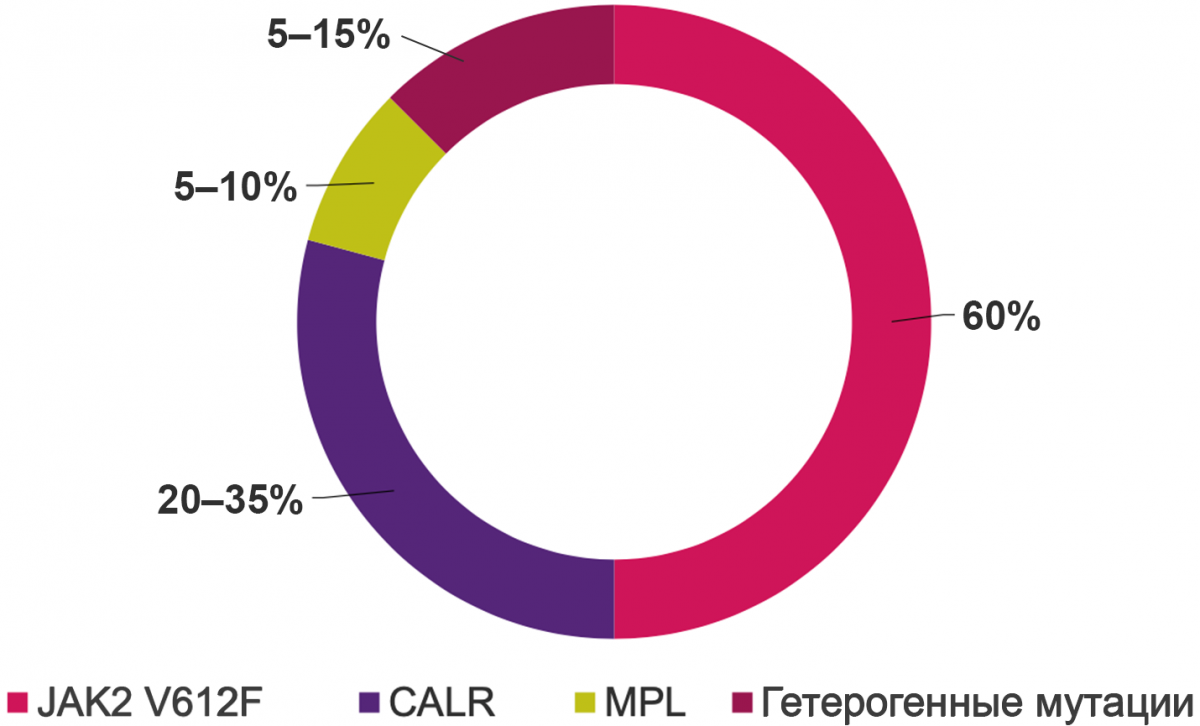
Рисунок 1. Частота различных мутаций при ПМФ2
Клиническая картина
Типичные клинические признаки ПМФ включают прогрессирующую анемию, симптоматическую спленомегалию как следствие экстрамедуллярного гемопоэза, симптомы опухолевой интоксикации и различные конституциональные симптомы (кахексию, пониженную температуру)3. Спленомегалия служит в качестве основной причины осложнений. Она вызывает раннее ощущение сытости, боль в животе и дискомфорт, одышку, кашель, иногда диарею. При отсутствии лечения спленомегалия приобретает прогрессирующий характер3.
Фазы ПМФ
В клиническом течении ПМФ выделяют фазы, отражающие степень прогрессирования заболевания: хроническая фаза, фаза акселерации, терминальная фаза бластной трансформации или бластный криз (табл. 1)4.
Таблица 1 — Фазы первичного миелофиброза4
| Хроническая фаза |
|
| Фаза акселерации |
|
| Бластный криз |
|
Стадии ПМФ
-
Префиброзная/ранняя стадия характеризуется гиперклеточностью костного мозга с расширением гранулоцитарного ростка, пролиферацией мегакариоцитарного ростка с атипией гистотопографии и структуры мегакариоцитов, отсутствием или минимальным ретикулиновым фиброзом (MF-0, MF-1 по Европейской системе градации).
-
Фиброзная стадия морфологически характеризуется ретикулиновым, коллагеновым фиброзом костного мозга или остеосклерозом (MF-2, MF-3 по Европейской системе градации), редукцией эритроидного ростка, выраженной атипией элементов мегакариоцитопоэза. Клиническая картина характеризуется спленомегалией, анемией, повышением концентрации ЛДГ, лейкоэритробластозом в гемограмме, появлением каплевидных эритроцитов.
Оценка степени фиброза костного мозга проводится по шкале от 0 до 35:
-
MF-0 редкие волокна ретикулина без пересечений, соответствующие нормальному костному мозгу;
-
MF-1 неплотная сеть ретикулина с множеством пересечений, особенно в периваскулярных зонах;
-
MF-2 диффузное увеличение плотности ретикулина с избыточными пересечениями, изредка с фокальными образованиями коллагена и/или фокальным остеосклерозом;
-
MF-3 диффузное увеличение плотности ретикулина с избыточными пересечениями с пучками коллагена, часто связанными со значительным остеосклерозом3.
Список литературы:
- Meier B., Burton J.H. Myeloproliferative Disorders. Hematol Oncol Clin North Am. 2017;31(6):1029‐1044. doi: 10.1016/j.hoc.2017.08.007
- Gilani J.A., Ashfaq M.A., Mansoor A.E. et al. Overview of the Mutational Landscape in Primary Myelofibrosis and Advances in Novel Therapeutics. Asian Pac J Cancer Prev. 2019;20(6):1691‐1699. Published 2019 Jun 1. doi: 10.31557/APJCP.2019.20.6.1691
- Tefferi A. Primary myelofibrosis: 2019 update on diagnosis, risk-stratification and management. Am J Hematol. 2018;93(12):1551‐1560. doi: 10.1002/ajh.25230
- NCCN Clinical Practice Guidelines in Oncology Myeloproliferative neoplasms version I.2020-May 21.2020.
- Thiele J et al. European consensus on grading bone marrow fibrosis and assessment of cellularity. Haematologica. — 2003. Vol. 90 № S. — P. 112S-1132.
746550/JAK/webpage/11.23/0
