Цели терапии
Предотвращение и лечение тромбогеморрагических осложнений1.
Контроль симптомов опухолевой интоксикации2.
Сведение к минимуму риска прогрессии (бластный криз, постполицитемический миелофиброз).
Предупреждение осложнений в случае беременности, хирургических операций3.
Методы терапевтического воздействия при истинной полицитемии
-
Профилактика тромботических осложнений:
-
антиагреганты: ацетилсалициловая кислота (100–500 мг/сут), клопидогрел (75 мг/сут).
-
-
Физическое удаление избыточной массы циркулирующих эритроцитов:
-
гемоэксфузии (кровопускания);
-
эритроцитаферез (ручной или аппаратный).
-
-
Циторедуктивная терапия:
-
гидроксикарбамид, 10–30 мг/кг/сут;
-
ИНФα, 1,5–5 млн МЕ 3 раза в неделю;
-
пегилированный ИНФα (пэгинтерферон α-2а, пэгинтерферон α-2b, цепэгинтерферон α-2b), 45–160 мкг 1 раз в неделю;
-
руксолитиниб;
-
бусульфан.
-
-
Лечение осложнений заболевания (тромбозы, тромбоэмболии).
-
Профилактика (контроль факторов риска) и лечение сердечно-сосудистых заболеваний3.
Алгоритм терапии истинной полицитемии4
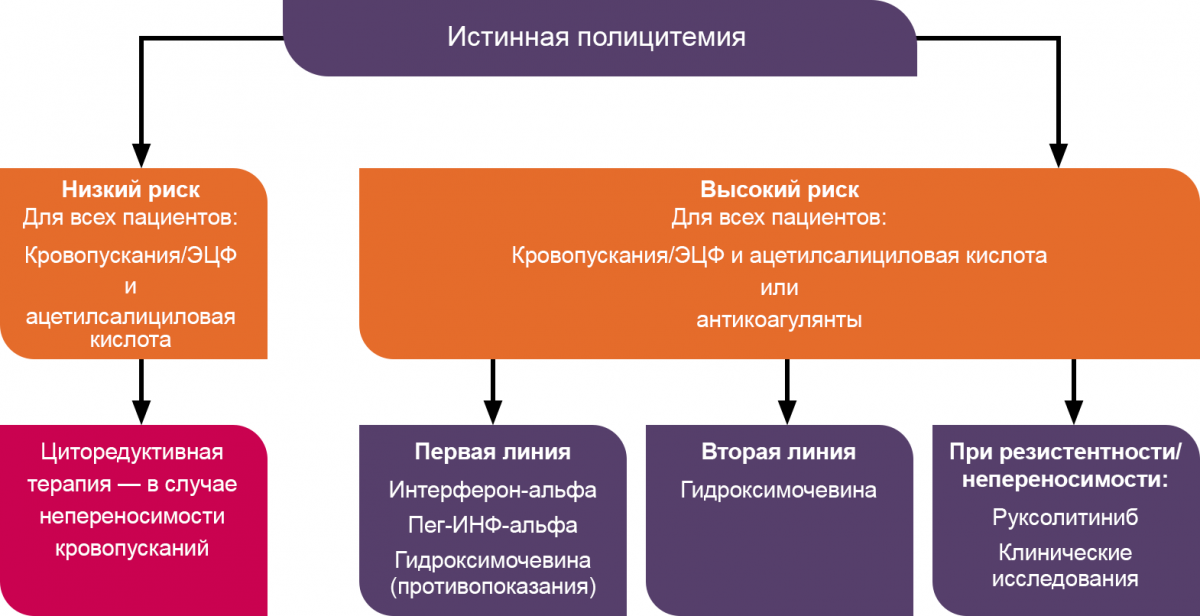
Профилактика тромботических осложнений:
1. Ацетилсалициловая кислота:
-
Снижает риски тромбоза по сравнению с плацебо (рис. 1).
-
У больных истинной полицитемией риск нефатального инфаркта миокарда, нефатального инфаркта мозга или смерти от сердечно-сосудистых причин, тромбоэмболии легочной артерии, большого венозного тромбоза или смерти от сердечно-сосудистых причин ниже при терапии ацетилсалициловой кислотой5.
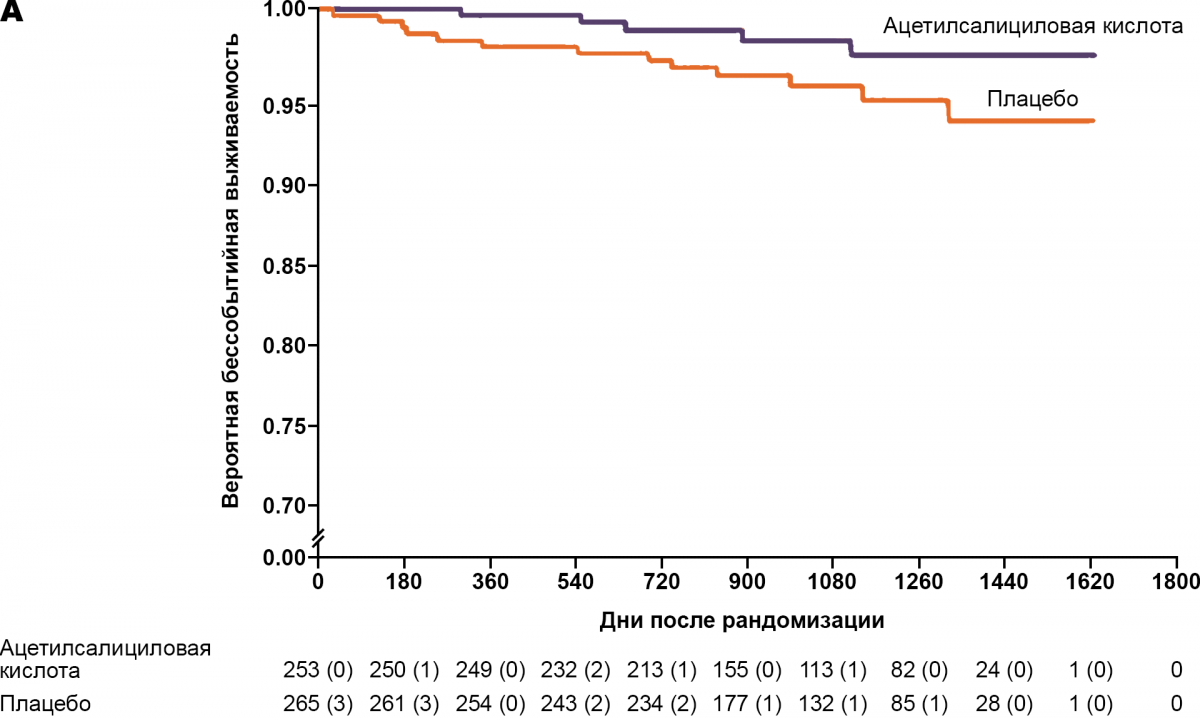
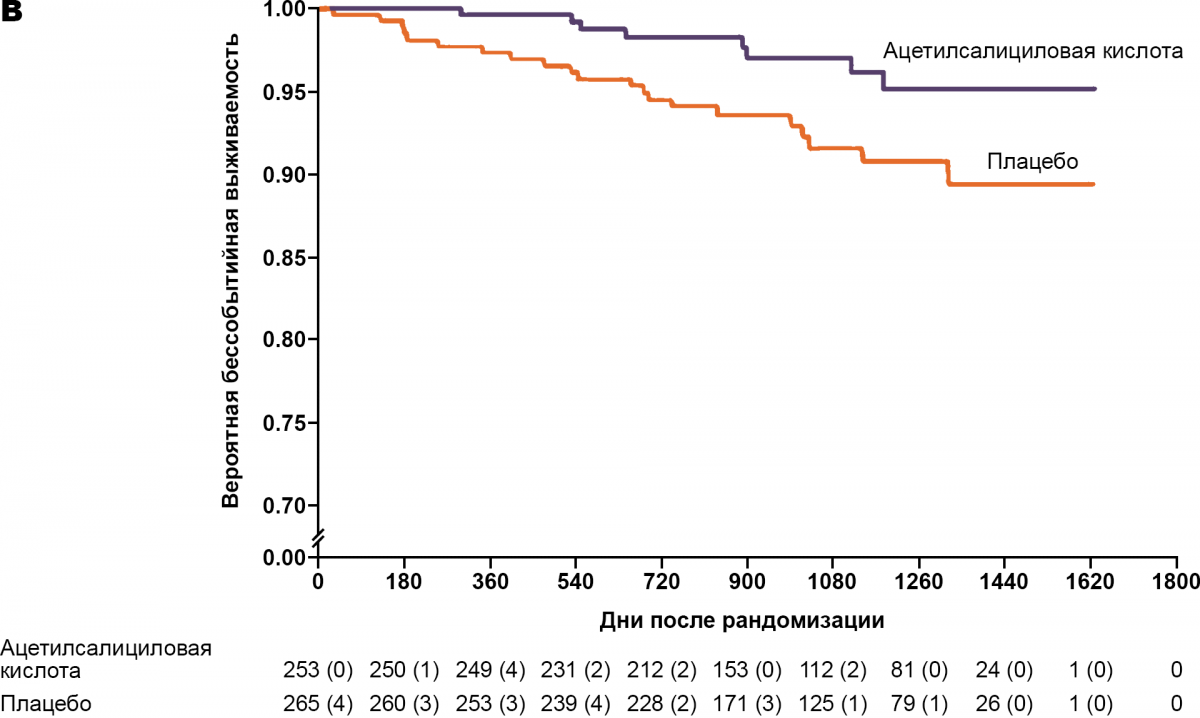
Рисунок 1. Вероятная выживаемость без инфаркта миокарда, инфаркта мозга и смерти от сердечно-сосудистых причин (рисунок A) и вероятность выживания без смерти от сердечно-сосудистых причин, ТЭЛА и тромбоза глубоких вен (рисунок B)
2. Физическое удаление избыточной массы циркулирующих эритроцитов с целью поддержания гематокрита менее 45%:
-
гемоэксфузии (кровопускания);
-
эритроцитаферез (ручной или аппаратный).
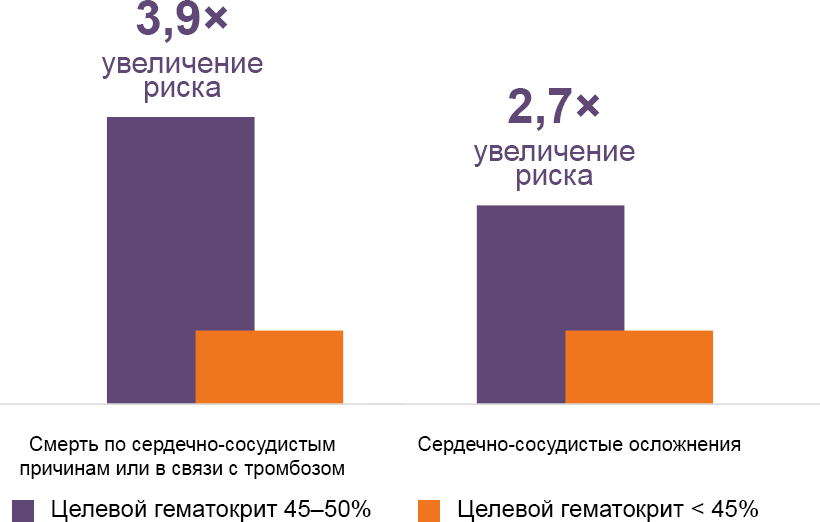
В проспективном рандомизированном клиническом исследовании CYTO-PV (Cytoreductive Therapy in Polycythemia Vera) с включением 365 больных показано, что частота смерти от сердечно-сосудистых и тромботических осложнений у больных при достижении целевого уровня гематокрита менее 45% в 4 раза ниже в сравнении с группой пациентов с уровнем гематокрита 45–50% (рис. 2, 3)5.
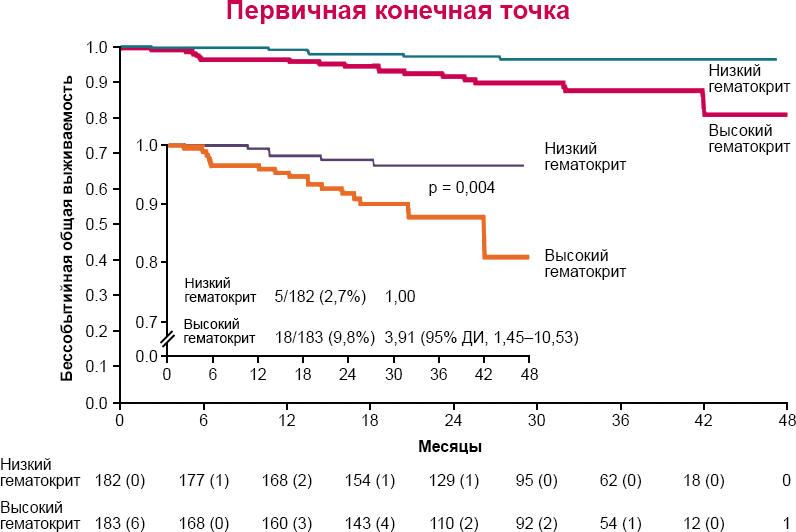
Рисунок 2. Результаты клинического исследования CYTO-PV: первичная конечная точка
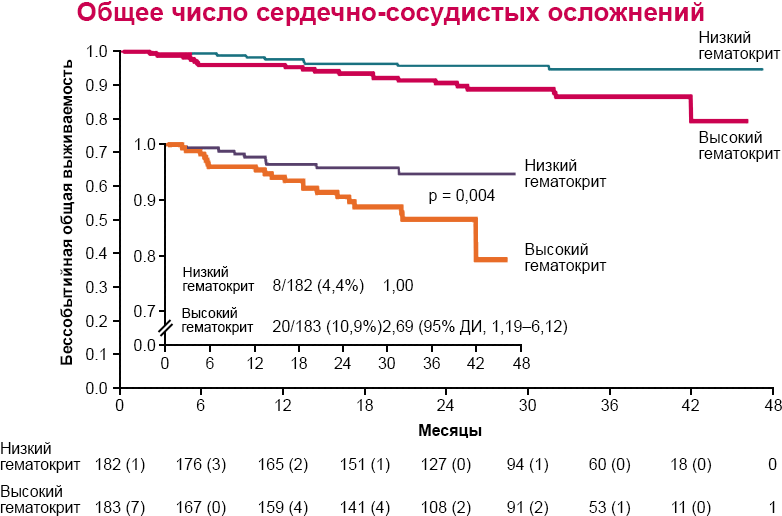
Рисунок 3. Результаты клинического исследования CYTO-PV: общее число сердечно-сосудистых осложнений
Гематокрит < 45% связан:
-
со снижением риска от сердечно-сосудистых осложнений в четыре раза;
-
со снижением частоты сердечно-сосудистых осложнений в три раза.
Критерием неэффективности кровопусканий является потребность в проведении процедур с частотой более чем 1 курс в 3 месяца. В случае неэффективности кровопусканий возрастает риск тромботических осложнений (рис. 4)6.
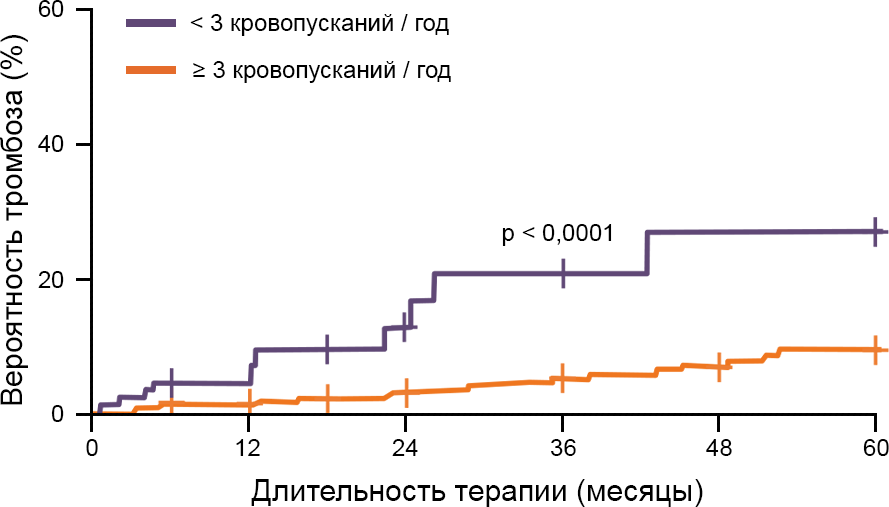
Рисунок 4. Влияние частоты кровопусканий на риск тромбозов
3. Циторедуктивная терапия
Циторедуктивная терапия проводится всем больным, отнесенным в группу высокого риска тромботических осложнений4,7,8.
Дополнительные факторы, влияющие на выбор варианта лечения:
-
Наличие и степень выраженности симптомов заболевания;
-
Массивная спленомегалия;
-
Высокие лейкоцитоз и тромбоцитоз;
-
Переносимость и эффективность кровопусканий/эритроцитафереза;
-
Сопутствующие заболевания и необходимость их постоянной терапии;
-
Образ жизни пациента4,7,8.
Выбор препарата для лечения истинной полицитемии определяется многими факторами: возраст, сопутствующие заболевания, доступность препарата, линия лечения (табл. 1)3,4,7,8,9,10.
Таблица 1 — Лечение истинной полицитемии3,4,7,8,9,10
| Параметр | Препарат | Дозировка |
| Первая линия терапии | Интерферон альфа-2b | По 3 млн МЕ через день, подкожно |
| Пегилированный интерферон альфа-2а | 180 мкг 1 раз в неделю, подкожно | |
| Пегилированный интерферон альфа-2b |
0,5 мл (при массе тела 54–66 кг), 0,6 мл (при массе тела 67–80 кг), 0,8 мл (при массе тела 81–106 кг), 1 мл (при массе тела 107–133 кг) 1 раз в неделю, подкожно |
|
| Гидроксикарбамид | 500–2000 мг 1 раз в день, однократно | |
| Непереносимость или резистентность гидроксикарбамида | Руксолитиниб | По 10 мг 2 раза в день |
| Возраст > 70 лет | Бусульфан | По 2–4 мг до суммарной дозировки 200 мг |
Вторая линия терапии истинной полицитемии
В случае отсутствия успеха лечения требуется смена препаратов3,4,7–10
-
Интерферон-α, при резистентности/непереносимости гидроксикарбамида;
-
Гидроксикарбамид, при резистентности/непереносимости интерферона-α;
-
Бусульфан, для пациентов с короткой вероятной продолжительностью жизни;
-
Пипоброман, 32Р (используется нечасто);
-
Руксолитиниб, у пациентов с неадекватным ответом или непереносимостью гидроксикарбамида;
-
Руксолитиниб, у пациентов с резистентностью или непереносимостью гидроксикарбамида.
Список литературы:
- Vannucci A. et al. Blood. 2007;110(3):840-6.
- Holly L. Geyer and Ruben A. Mesa Blood. Blood First Edition Paper, prepublished online December 3, 2014; doi: 10.1182/blood-2014-05-577635
- Меликян А.Л., Туркина А.Г., Ковригина А.М. и др. Клинические рекомендации по диагностике и терапии Ph-негативных миелопролиферативных заболеваний (истинная полицитемия, эссенциальная тромбоцитемия, первичный миелофиброз) (редакция 2016 г.). Гематология и трансфузиология 2017; 1:25—60.
- Barbui T. et al. Philadelphia chromosome-negative classical myeloproliferative neoplasms: revised management recommendations from European LeukemiaNet. Leukemia. 2018 May;32(5):1057-1069. doi: 10.1038/s41375-018-0077-1
- Marchioli R., Finazzi G., Specchia G. et al. The CYTO-PV: a large-scale trial testing the intensity of CYTO-reductive therapy to prevent cardiovascular events in patients with Polycythemia Vera. Thrombosis. 2011;2011:794240. doi: 10.1155/2011/794240
- Alvarez-Larrán A. et al. Haematologica. 2016.
- Mesa R.A., Jamieson C., Bhatia R. et al. NCCN Guidelines Insights: Myeloproliferative Neoplasms, Version 2.2018. J Natl Compr Canc Net. 2017 Oct;15(10):1193-1207. doi: 10.6004/jnccn.2017.0157
- Heidel F.H., Gale R.P., Hochhaus Managing myeloproliferative neoplasms evidence based on the ELN treatment recommendations 2018. A.Leukemia. 2018 May;32(5):1055-1056. doi: 10.1038/s41375-018-0079-z
- Foucar C.E., Stein B.L. Contemporary Use of Interferon Therapy in the Myeloproliferative Neoplasms. Curr Hematol Malig Rep. 2017 Oct;12(5):406-414. doi: 10.1007/s11899-017-0402-1
- Forsyth C.J., Chan W.H., Grigg A.P., Cook N.C., Lane S.W., Burbury K.L., Perkins A.C., Ross D.M. Recommendations for the use of pegylated interferon-alpha in the treatment of classical myeloproliferative neoplasms. Intern Med J. 2019;49(8):948-954. doi: 10.1111/imj.14154
732635/JAK/webpage/10.23/0
