Новости ASCO 2023
Эффективность и безопасность алпелисиба у пациентов c HR+ HER2– рРМЖ с мутацией PIK3CA: результаты анализа 3 когорт исследования BYLieve1
Эффективность и безопасность алпелисиба у пациентов с HR+ HER2– рРМЖ с мутацией гена PIK3CA, у которых заболевание прогрессировало во время или после предшествующей терапии, включая лечение ингибиторами CDK4/6, изучали в исследовании II фазы BYLieve, включавшей 3 когорты пациентов (рис. 1 ):
- в когорте А пациенты получали алпелисиб с фулвестрантом после прогрессирования на фоне терапии ингибитором CDK4/6 с летрозолом;
- в когорте B пациенты получали алпелисиб с летрозолом после прогрессирования на фоне терапии ингибитором CDK4/6 с фулвестрантом. В настоящее время алпелисиб на зарегистрирован в комбинации с летрозолом для лечения РМЖ.
- в когорте С пациенты получали алпелисиб с фулвестрантом после прогрессирования на химиотерапии (ХТ) или ЭТ.
Рисунок 1. Исследование II фазы BYLieve: критерии включения, описание трёх когорт и конечные точки исследования.
На конгрессе ASCO 2023 были представлены обновлённые данные об эффективности и безопасности алпелисиба в сочетании с ЭТ через 18 месяцев наблюдения всех когорт пациентов в исследовании BYLieve1. Подробно остановимся на данных когорты А и С, где алпелисиб назначался в зарегистрированной комбинации с фулвестрантом.
Таблица 1. Демографические и исходные характеристики
|
|
Когорта А |
Когорта С |
|---|---|---|
|
Медиана возраста (годы) |
58.0 (33.0-83.0) |
58.0 (31.0-84.0) |
|
Медиана ИМТ, кг/м 2 |
119 25.30 (16.10-46.60) |
122 25.35 (16.70-45.10) |
|
Менопаузальный статус |
||
|
пременопауза |
22 (17.3) |
18 (14.3) |
|
постменопауза |
105 (82.7) |
107 (84.9) |
|
ECOG |
||
|
0 |
81 (63.8) |
71 (56.3) |
|
1 |
41 (32.3) |
49 (38.9) |
|
2 |
2 (1.6) |
4 (3.2) |
|
Нет данных |
3 (2.4) |
2 (1.6) |
|
Локализация мтс |
||
|
Кости |
109 (85.8) |
92 (73.0) |
|
Только кости |
23 (18.1) |
15 (11.9) |
|
Висцеральные |
86 (67.7) |
93 (73.8) |
|
Легкие |
43 (33.9) |
48 (38.1) |
|
Печень |
60 (47.2) |
69 (54.8) |
|
Другие висцеральные мтс |
8 (6.3) |
7 (5.6) |
|
Лимфоузлы |
38 (29.9) |
44 (34.9) |
|
Другая локализация |
12 (9.4) |
13 (10.3) |
|
Линии предшествующей терапии мРМЖ
|
||
|
0 |
2 (1.6) |
2 (1.6) |
|
1 |
101 (79.5) |
44 (34.9) |
|
2 |
23 (18.1) |
77 (61.1) |
|
≥ 3 |
1 (0.8) |
3 (2.4) |
|
Предшествующая линия терапии |
||
|
Таргетная терапия |
115 (90.6) |
36 (28.6) |
|
Гормонотерапия |
99 (78.0) |
69 (54.8) |
|
ХТ |
0 |
46 (36.5) |
Пациенты, включенные в исследование, имели высокую опухолевую нагрузку: висцеральные мтс отмечались у 66.7% пациентов в Когорте A и у 73.8% в Когорте С; только костные мтс были у 18.1% и 11.9% пациентов в Когортах A и C, соответственно. Две и более предшествующих линий терапии мРМЖ получили 18.9% и 63.5% пациентов в Когортах A и C, соответственно.
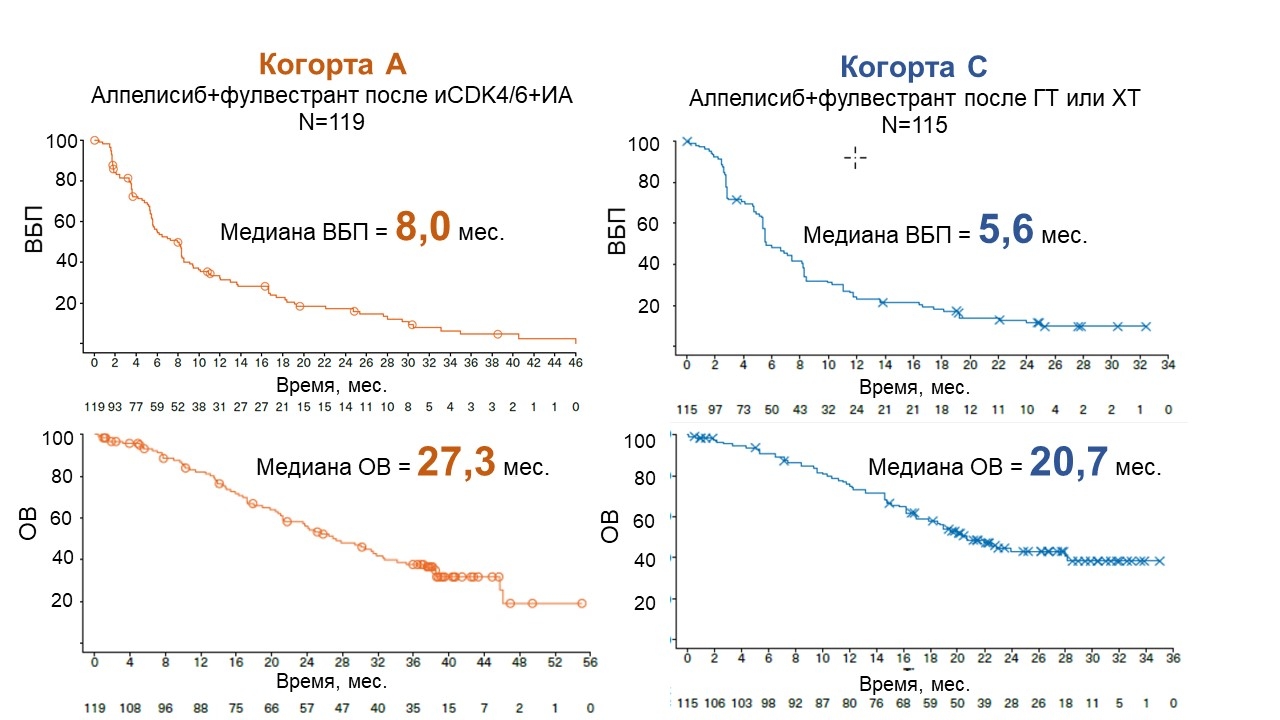
Долгосрочное наблюдение пациентов и накопление событий позволили уточнить значение медианы ВБП в когорте А – 8,0 мес. и оценить эффективность следующей после алпелисиба линии терапии по ВБП2.
|
Когорта А |
Когорта С |
|
|---|---|---|
|
мВБП |
8,0 мес. |
5,6 мес. |
|
мВБП2 |
15,2 мес. |
13,5 мес. |
|
мОВ |
27,3 мес. |
20,7 мес. |
Рисунок 2. ВБП (а) и ОВ (б) в когортах A и С исследования BYLieve.
Важно отметиться, что пациенты, получавшие алпелисиб во 2-ой линии сразу после ингибитора CDK4/6, имели численное преимущество в мОВ перед пациентами, получавшими алпелисиб в 3-ей линии:
|
2 линия, n=95 |
3 линия, n=22 |
|
|---|---|---|
|
мВБП, мес. |
8,1 (5,6-9,5) |
8,0 (3,6-18,4) |
|
мОВ, мес. |
27,8 (21,3-37,3) |
21,3 (15,4-32,7) |
Безопасность
Наиболее частыми нежелательными явлениями (НЯ) любой степени тяжести во всех когортах были диарея (64,6%; 68,3%; 54,0%), гипергликемия (59,8%; 65,1%; 67,5%), тошнота (46,5%; 54,8%; 40,5%), сыпь (31,5%; 31,0%; 40,5%) и утомляемость (30,7%; 31,0%; 34,9%).
Через 1 месяц после начала лечения алпелисибом частота и тяжесть НЯ, представляющих особый интерес, таких как гипергликемия, диарея и сыпь, значительно снижалась (рис. 3).
Рисунок 3. Частота возникновения НЯ, представляющих особый интерес, с течением времени от начала лечения в исследовании BYLieve: (а) гипергликемия, (б) диарея и (в) сыпь13.
Уровень глюкозы в плазме натощак (ГПН) у пациентов во всех 3 когортах повышался после начала приема алпелисиба, достигая пиковых уровней к 15-му дню 1-го цикла, но затем стабилизировался, независимо от исходного статуса (нормального или преддиабетического состояния) (рис. 4).
Рисунок 4. Изменение уровня ГПН (95% ДИ) с течением времени у пациентов с нормальным или преддиабетическим статусом в когорте А.
Заключение:
Представленные на ASCO 2023 результаты 1,5 летнего наблюдения за пациентами из 3 когорт исследования BYLieve показывают, что комбинация алпелисиба с ЭТ может быть эффективным лечением пациентов с HR+ HER2– рРМЖ с мутацией гена PIK3CA при прогрессировании во время или после предшествующего лечения, в том числе ингибиторами CDK4/6. Пациенты, получавшие алпелисиб во 2-ой линии сразу после ингибиторов CDK4/6, имели численное преимущество в мОВ перед пациентами, получавшими алпелисиб в 3-ей линии, что потенциально демонстрирует повышенную клиническую пользу лечения алпелисибом в более ранних линиях.
НЯ соответствовали хорошо охарактеризованному, управляемому и предсказуемому профилю безопасности алпелисиба; никаких новых сигналов безопасности не наблюдалось ни в одной из когорт. Снижение частоты гипергликемии всех степеней, диареи и сыпи с течением времени позволяют предположить, что принятые в клинической практике стратегии профилактики, лечения и мониторинга НЯ могут способствовать увеличению продолжительности лечения алпелисибом.
Опубликованные ранее данные указывают на эффективность профилактики гипергликемии и сыпи2-4. Оценить исходный риск и выбрать схему коррекции гипергликемии можно на сайте АОР:
Литература:
- Chia S, et al. Alpelisib + endocrine therapy in patients with PIK3CA-mutated, hormone receptor–positive, human epidermal growth factor receptor 2–negative, advanced breast cancer: Analysis of all 3 cohorts of the BYLieve study. J Clin Oncol. 2023 41:16_suppl, 1078-1078.
- Filonenko D. and Zhukova L. Prophylactic use of metformin in patients on alpelisib treatment. Journal of Clinical Oncology 2022 40:16_suppl, e13040-e13040.
- Borrego et al. Metformin (MET) for the prevention of alpelisib (ALP)-related hyperglycemia (HG) in PIK3CA-mutated, hormone receptor-positive (HR[+]) HER2-negative (HER2[-]) advanced breast cancer (ABC): The METALLICA study. SABCS Dec 6-10, 2022. PD8-02.
- Rugo H et al. Time course and management of key adverse events during the randomized phase III SOLAR-1 study of PI3K inhibitor alpelisib plus fulvestrant in patients with HR-positive advanced breast cancer. Ann Oncol. 2020;31(8):1001-1010.
- Алгоритм по профилактике и коррекции сыпи доступен он-лайн на сайте АОР: https://oncology-association.ru/calc/sip.html
11247350/ALP/web/08.24/0