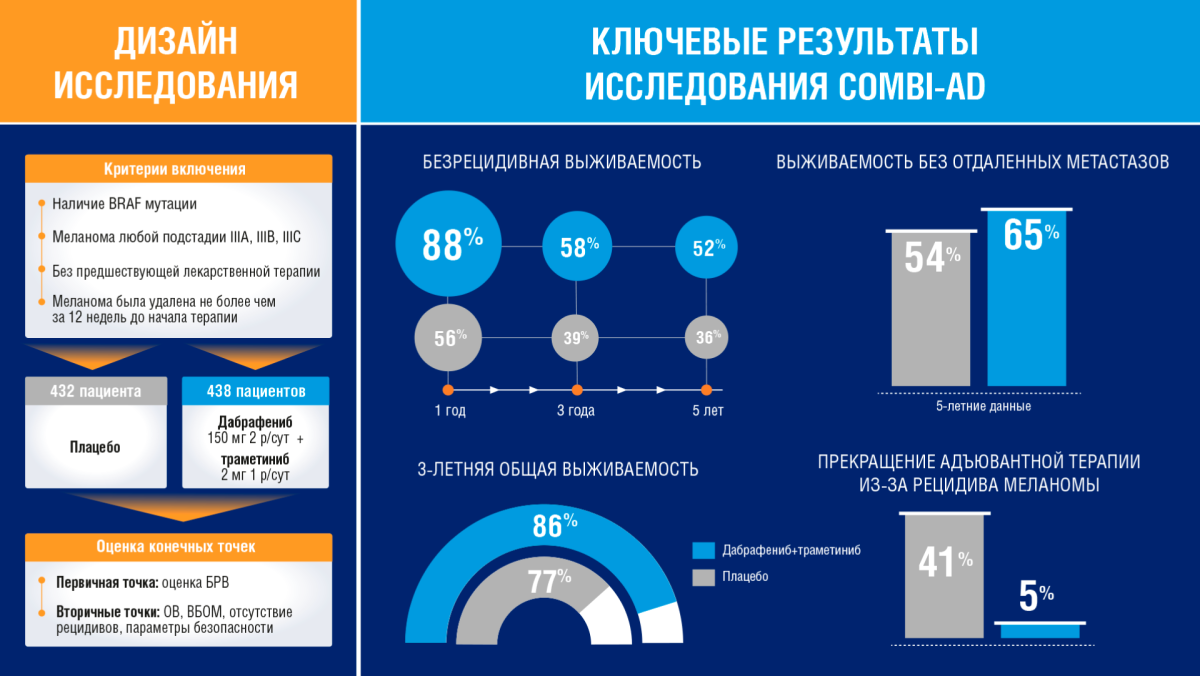
COMBI-AD —это международное рандомизированное двойное слепое плацебо-контролируемое исследование, в котором оценивали эффект от адъювантной терапии комбинацией дабрафениб + траметиниб по сравнению с плацебо у 870 пациентов с резецированной меланомой с мутацией BRAF V600 на стадии IIIA, IIIB или IIIC (рис. 1).
Дизайн исследования
В исследовании приняли участие 870 пациентов из 169 центров в 25 странах.
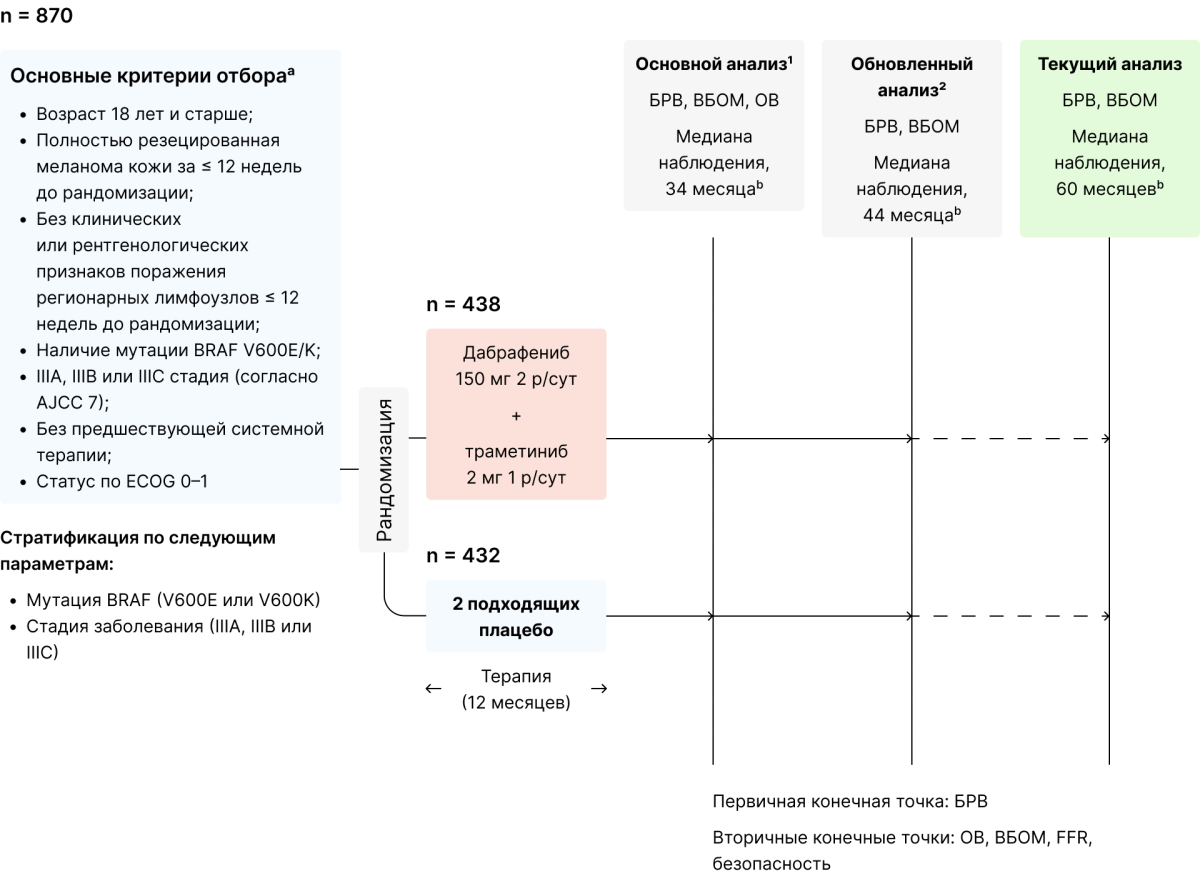
Рисунок 1. Дизайн исследования COMBI-AD
Пациенты получали дабрафениб в дозе 150 мг два раза в день и траметиниб в дозе 2 мг один раз в день или две соответствующие таблетки плацебо. Пациенты были стратифицированы в соответствии с их статусом мутации BRAF (V600E или V600K) и стадией заболевания (IIIA, IIIB или IIIC). Лечение длилось 12 месяцев при отсутствии рецидива заболевания, неприемлемой токсичности, отзыва согласия или смерти. Наблюдение за рецидивированием продолжалось до тех пор, пока не констатировался первый рецидив, после этого пациенты наблюдались на предмет выживаемости. Изменения дозы или перерывы требовались при негематологических нежелательных явлениях 2-й степени или выше, которые не поддавались лечению с помощью обычной поддерживающей терапии [2].
Таблица 1 — Распределение пациентов в исследовании COMBI-AD по стадиям заболевания согласно AJCC 7 изд.

Основные цели исследования
Первичной конечной точкой была безрецидивная выживаемость (БРВ), определяемая как время от рандомизации до рецидива заболевания или смерти от любой причины.
Вторичные конечные точки включали общую выживаемость (ОВ), выживаемость без отдаленных метастазов (ВБОМ) (время от рандомизации до даты первого отдаленного метастазирования или даты смерти, в зависимости от того, что произошло раньше), отсутствие рецидива (время от рандомизации до рецидива, с поправкой на пациентов, которые умерли от причин, отличных от меланомы или токсических эффектов, связанных с лечением) и безопасность терапии.
Результаты
Первичная конечная точка
На момент отсечения данных (8 ноября 2019 г.) 278 пациентов (63%) в группе комбинированной терапии и 234 (54%) в группе плацебо оставались под наблюдением. Показатели безрецидивной выживаемости составили 88% через 1 год, 67% через 2 года и 58% через 3 года в группе комбинированной терапии, по сравнению с показателями 56%, 44% и 39% соответственно в группе плацебо. Через 5 лет процент пациентов, которые были живы без рецидива, составил 52% (95% ДИ от 48 до 58) в группе комбинированной терапии и 36% (95% ДИ от 32 до 41) в группе плацебо (рис. 2) [1].
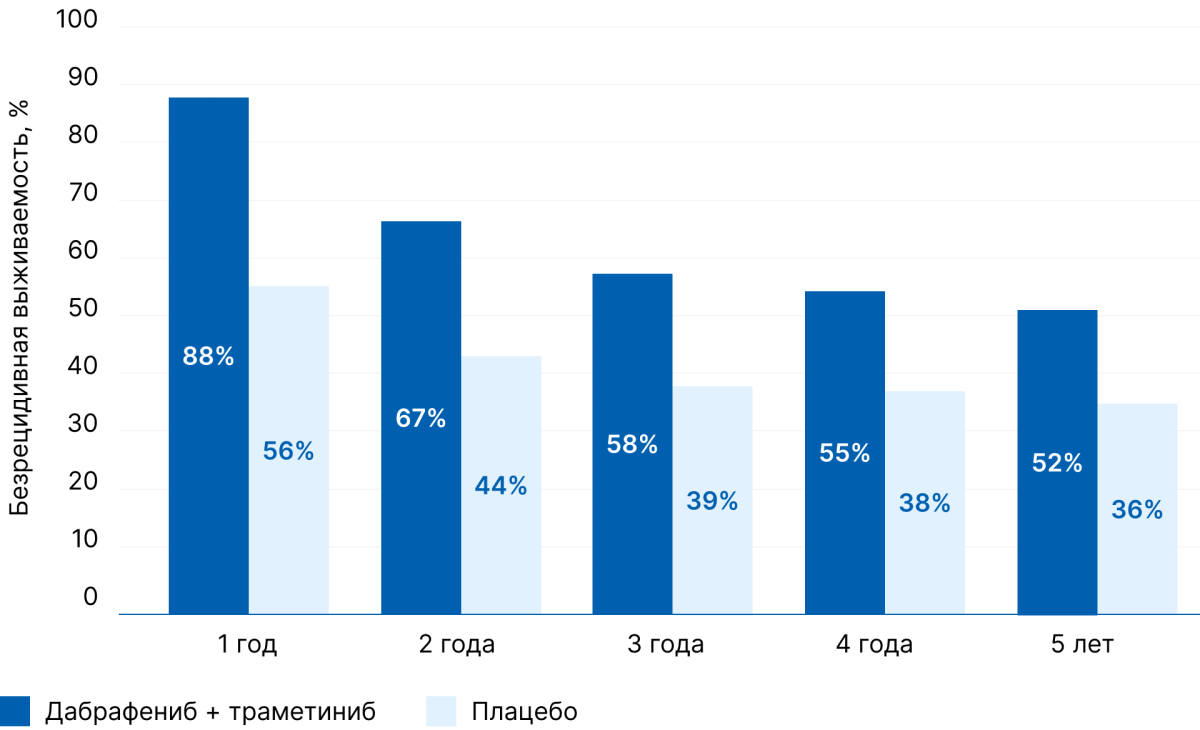
Рисунок 2. Безрецидивная выживаемость в группах сравнения в течение 5 лет
Безрецидивная выживаемость была выше при применении дабрафениба и траметиниба, чем при применении плацебо, независимо от подстадий меланомы (рис. 3) [1,3].
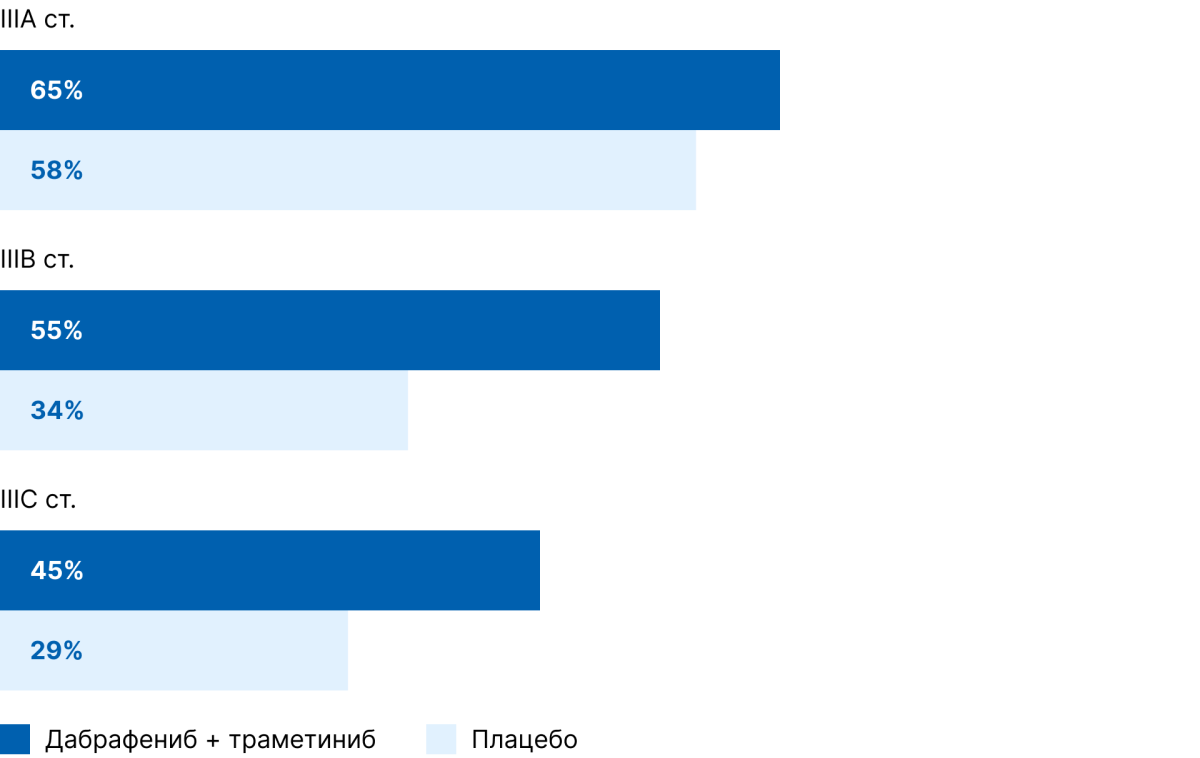
Рисунок 3. 5-летняя безрецидивная выживаемость в зависимости от подстадии меланомы кожи
Прекращение адъювантной терапии из-за рецидива меланомы
Всего 5% пациентов прекращали адъювантную терапию комбинацией дабрафениб + траметиниб в связи с возникновением рецидива, в отличие от адъювантной иммунотерапии, где процент отмены терапии из-за рецидива составил от 21% до 27% (рис. 4).
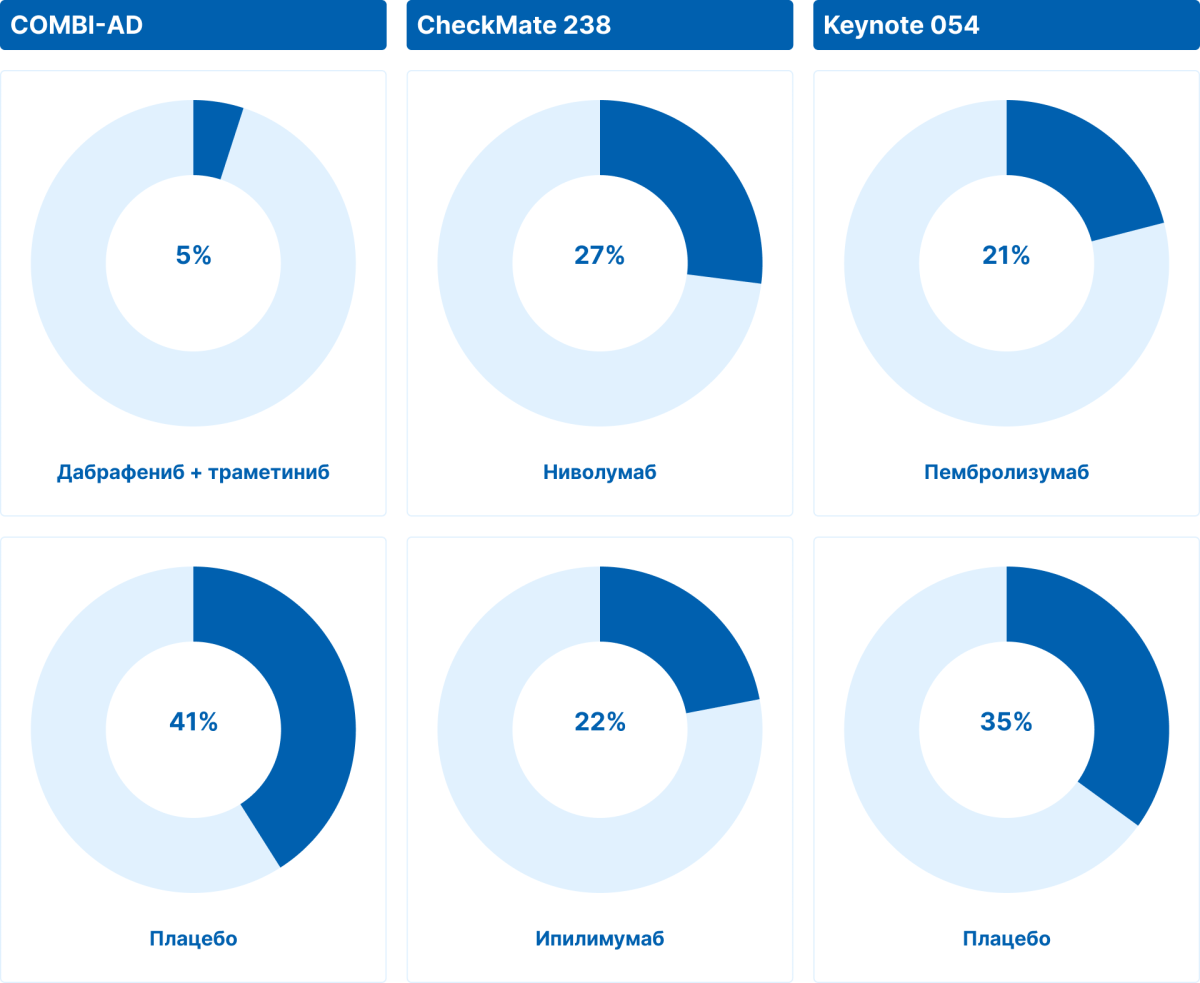
Рисунок 4. Прекращение адъювантной терапии из-за рецидива меланомы
Таким образом, применение дабрафениба и траметиниба увеличивало безрецидивную выживаемость среди всех пациентов III стадии как в краткосрочном, так и в долгосрочном периоде. Стоит отметить, что комбинация дабрафениб + траметиниб снижала риск рецидива во всех клинических подгруппах, вне зависимости от изъязвления опухоли, наличия макрометастазов и числа пораженных л/у [1].
Вторичные конечные точки
Общая выживаемость
Анализ общей выживаемости был представлен с охватом наблюдения в 3 года [3]. На момент подсчета данных 5-летнего наблюдения за пациентами летальность не превысила 50%, в связи с чем общая выживаемость в нем не анализировалась [1].
Общая выживаемость составила 97% через 1 год, 91% через 2 года и 86% через 3 года в группе комбинированной терапии, по сравнению с показателями 94%, 83% и 77% соответственно в группе плацебо (рис. 5) [3].
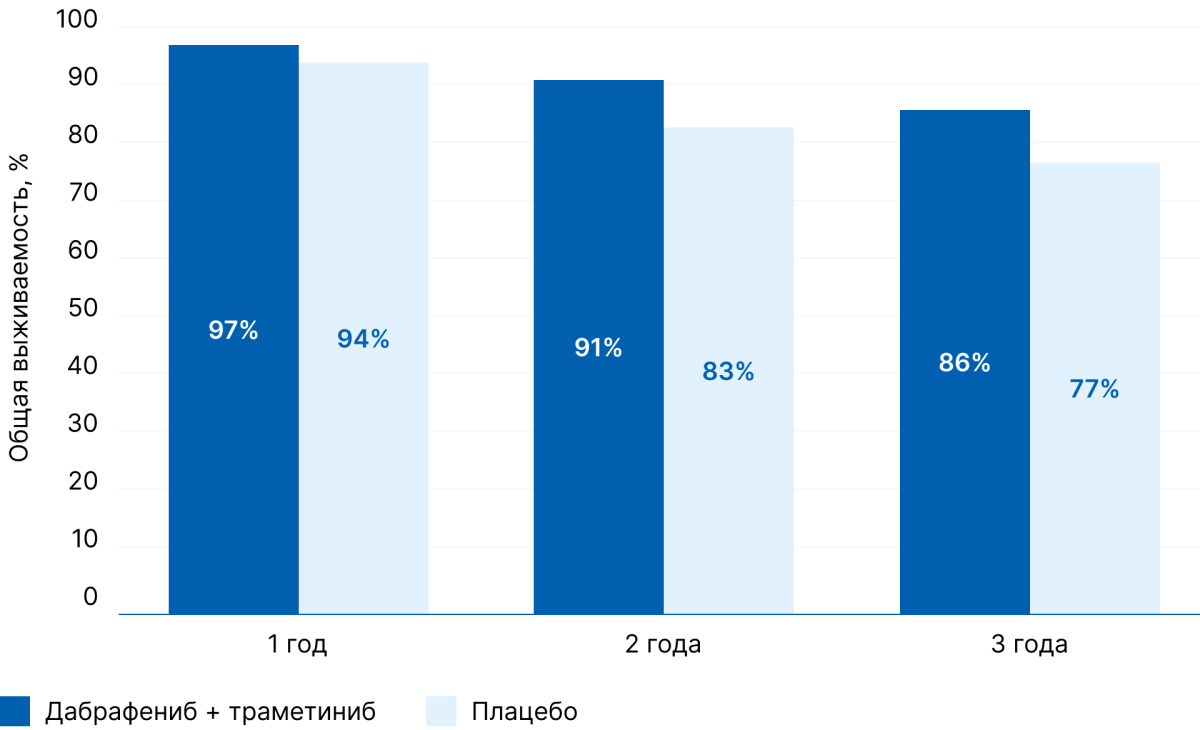
Рисунок 5. Общая выживаемость в группах сравнения в течение первых 3 лет [3]
Исследование и наблюдение продолжаются. Следующий анализ общей выживаемости будет проведен, когда произойдет 50% событий [1,2].
Таким образом, общая выживаемость в течение 3 лет была выше в группе пациентов, получавших терапию дабрафенибом и траметинибом, по сравнению с группой плацебо.
Выживаемость без отдаленных метастазов (ВБОМ)
Через 5 лет от начала исследования были живы и не имели отдаленных метастазов 65% пациентов в группе комбинированной терапии и 54% в группе плацебо. При этом медиана ВБОМ не была достигнута у пациентов из обеих групп. Для терапии дабрафенибом и траметинибом по сравнению с плацебо отношение рисков (ОР) отдаленного метастазирования или гибели составило 0,55 (95% ДИ от 0,44 до 0,70), таким образом, риск метастазирования или смерти снижался на 45% [1].
На ASCO 2022 года были опубликованы данные по выживаемости без отдаленных метастазов среди пациентов с разными стадиями заболевания (согласно AJCC 8 изд.). Через 5 лет частота ВБОМ была значительно выше у пациентов с более развитой стадией, особенно это заметно для пациентов с IIID стадией, где терапия дабрафенибом и траметинибом помогла снизить риск на 80% (рис. 6) [8].
Выживаемость без отдаленных местастазов
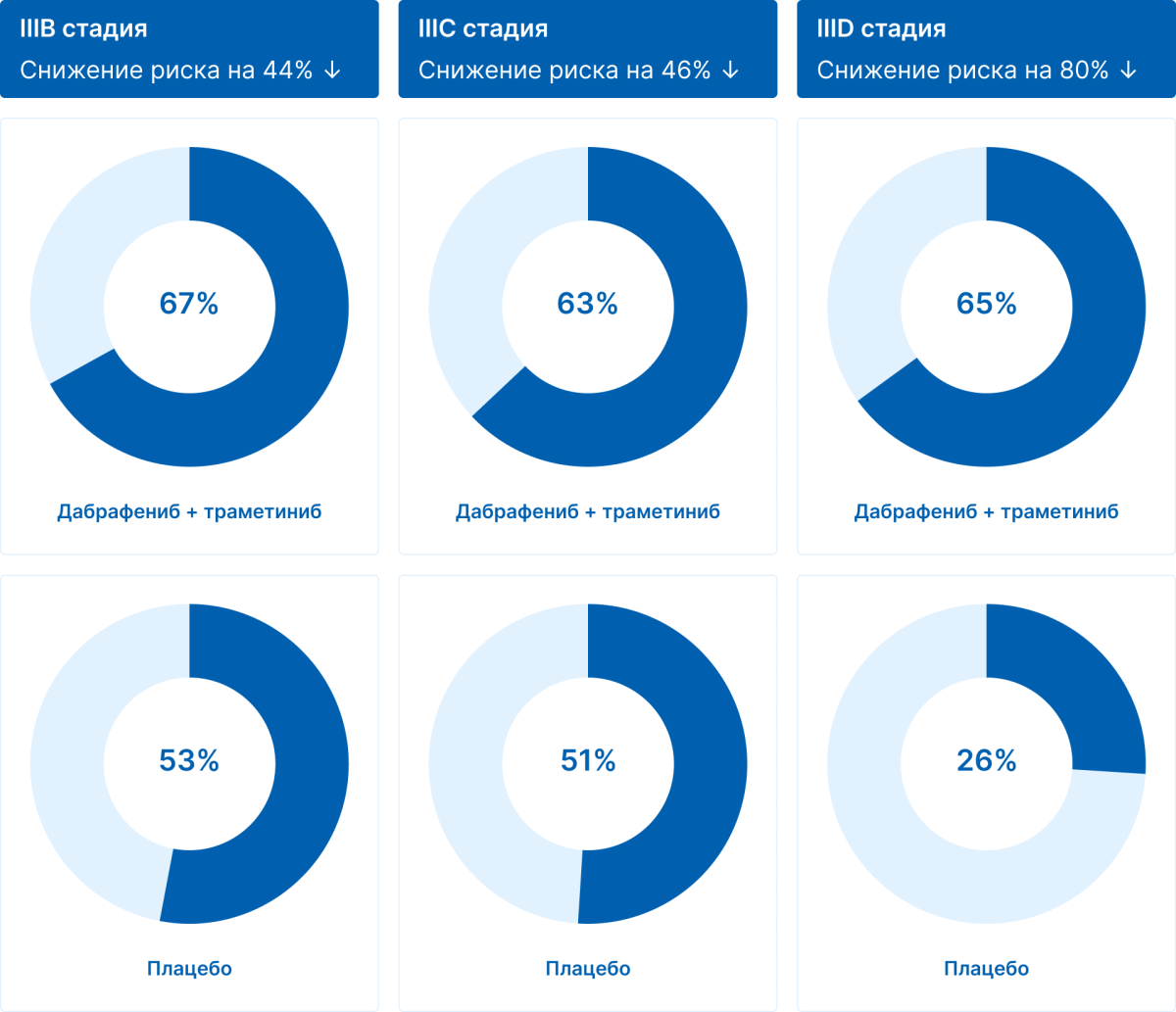
Рисунок 6. Выживаемость без отдаленных метастазов среди пациентов с разными подстадиями заболевания согласно AJCC 8 изд.
Безопасность
Всего в анализ безопасности были включены 435 пациентов в группе комбинированной терапии и 432 пациента в группе плацебо. Как минимум одно нежелательное явление было зарегистрировано у 422 пациентов (97%) в группе комбинированной терапии и у 380 пациентов (88%) в группе плацебо. Из нежелательных явлений у пациентов в группе комбинированной терапии наиболее частыми были лихорадка (любая степень, 63%; 3 или 4 степень, 5%), утомляемость (любая степень, 47%; 3 или 4 степень, 4%) и тошнота (любая степень, 40%; 3 или 4 степень, 1%) (табл. 2). Почти все нежелательные явления, которые были связаны с дабрафенибом и траметинибом, были преходящими и разрешались после временного или постоянного прекращения лечения.
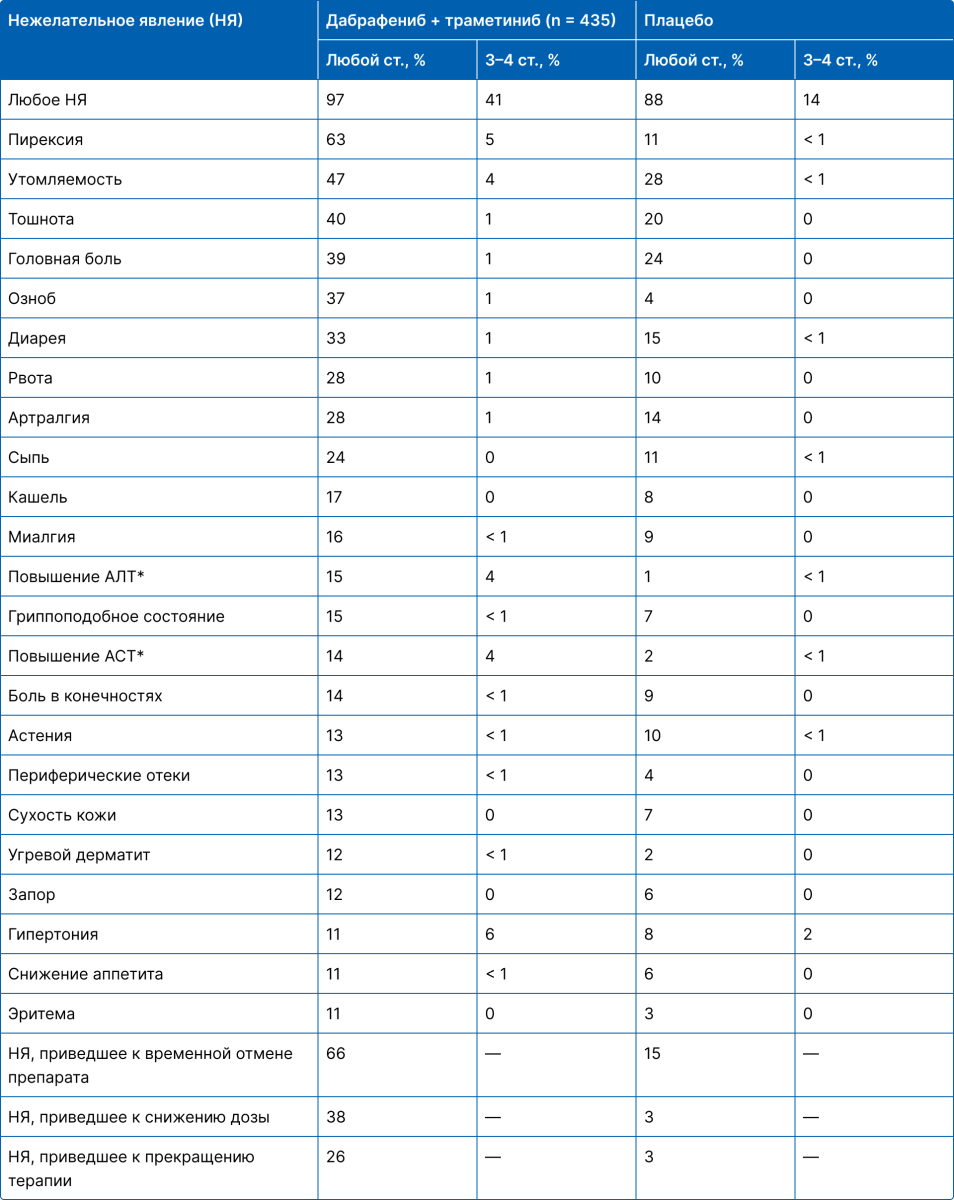
Примечание.
* АЛТ — аланинаминотрансфераза крови, АСТ — аспартатаминотрансфераза крови.
Наиболее частыми нежелательными явлениями, связанными с комбинированной терапией, были пирексия и утомляемость, что согласуется с данными предыдущих исследований терапии дабрафенибом и траметинибом пациентов с неоперабельной меланомой IIIC стадии или метастатической меланомой IV стадии [4–6]. Пирексия, как правило, развивалась в течение первого месяца лечения, длилась около трех дней и была управляемой, при этом не оказывала значительного влияния на качество жизни пациентов [10].
Стоит отметить, что частота пирексии в реальной клинической практике гораздо ниже. Так, в исследовании, представленном на EADO в 2021 году, было показано, что частота встречаемости пирексии составила всего лишь 35% — практически в 2 раза ниже, чем в исследовании COMBI-AD (рис. 7) [9].

Рисунок 7. Сравнение частоты пирексии в реальной клинической практике и исследовании COMBI-AD
Кроме того, тактика ведения пациентов с пирексией в последние годы была изменена и представлена в виде адаптированного алгоритма в исследовании COMBI-APlus [7], в настоящее время алгоритм включен в консенсусы и клинические рекомендации, а также в официальную инструкцию к препаратам [11–14]. Новый, адаптированный алгоритм управления пирексией позволил улучшить переносимость и повысить эффективность терапии [7].
Заключение
- Терапия дабрафенибом и траметинибом снижает риск рецидива на 49% в течение 5-летнего периода у пациентов с BRAF+ меланомой III стадии вне зависимости от характеристик опухоли.
- Терапия дабрафенибом и траметинибом уменьшает риск появления отдаленных метастазов через 5 лет после начала лечения на 45%.
- Всего 5% пациентов прекращали адъювантную терапию дабрафенибом и траметинибом в связи с возникновением рецидива меланомы.
- 3-летняя общая выживаемость при применении дабрафениба и траметиниба составила 86%. Медиана ОВ еще не достигнута.
- НЯ в группе дабрафениба и траметиниба были обратимы и контролируемы и не влияли на качество жизни пациентов.
Источники:
- Dummer R., Hauschild A., Santinami M. et al. Five-Year Analysis of Adjuvant Dabrafenib plus Trametinib in Stage III Melanoma. N Engl J Med. 2020;383(12):1139-1148. doi:10.1056/nejmoa2005493
- Hauschild A., Dummer R., Schadendorf D. et al. Longer follow-up confirms relapse-free survival benefit with adjuvant dabrafenib plus trametinib in patients with resected BRAF V600—mutant stage III melanoma. J Clin Oncol. 2018;36(35):3441-3449. doi:10.1200/JCO.18.01219
- Long G.V., Hauschild A., Santinami M. et al. Adjuvant Dabrafenib plus Trametinib in Stage III BRAF -Mutated Melanoma. N Engl J Med. 2017;377(19):1813-1823. doi:10.1056/nejmoa1708539
- Robert C., Karaszewska B., Schachter J. et al. Improved Overall Survival in Melanoma with Combined Dabrafenib and Trametinib. N Engl J Med. 2015;372(1):30-39. doi:10.1056/nejmoa1412690
- Flaherty K.T., Infante J.R., Daud A., Gonzalez R., Kefford R.F., Sosman J., ... & Weber J. Combined BRAF and MEK inhibition in melanoma with BRAF V600 mutations. N Engl J Med. 2012;367(18):1694-1703. doi:10.1056/NEJMoa1210093.Combined
- Robert C., Karaszewska B., Schachter J. et al. Two year estimate of overall survival in COMBI-v, a randomized, open-label, phase III study comparing the combination of dabrafenib (D) and trametinib (T) with vemurafenib (Vem) as first-line therapy in patients (pts) with unresectable or metastatic BRAF . Eur J Cancer. 2015;51(August):S663. doi:10.1016/s0959-8049(16)31820-2
- Atkinson V., Robert C., Grob J.J. et al. Improved pyrexia-related outcomes associated with an adapted pyrexia adverse event management algorithm in patients treated with adjuvant dabrafenib plus trametinib: Primary results of COMBI-APlus. Eur J Cancer. 2022;163:79-87. doi:10.1016/j.ejca.2021.12.015
- Schadendorf D. et al. Adjuvant dabrafenib plus trametinib (D + T) versus placebo in patients with resected stage III BRAFV600-mutant melanoma: Updated 5-year distant metastases-free survival (DMFS) analysis of COMBI-AD. — J Clin Oncol 40, 2022 (suppl 16; abstr 9563)/. doi: 10.1200/JCO.2022.40.16_suppl.9563
- Pattipaka T. et al. Real-world characterization of pyrexia in melanoma patients treated with dabrafenib and trametinib. Presented at WCM/EADO 2021.
- Schadendorf D. et al. Patient-reported outcomes in patients with resected, high-risk melanoma with BRAFV600E or BRAFV600K mutations treated with adjuvant dabrafenib plus trametinib (COMBI-AD): a randomised, placebo-controlled, phase 3 trial //The Lancet Oncology. — 2019. — Т. 20. — №. 5. — С. 701-710.
- Thawer A., Miller W.H. Jr, Gregorio N., Claveau J., Rajagopal S., Savage K.J., Song X., Petrella T.M. On Behalf Of The Canadian Working Group. Management of Pyrexia Associated with the Combination of Dabrafenib and Trametinib: Canadian Consensus Statements. Curr Oncol. 2021 Sep 14;28(5):3537-3553. doi: 10.3390/curroncol28050304. PMID: 34590600; PMCID: PMC8482100.
- Atkinson V., Long G., Menzies A., McArthur G., Carlino M.S., Millward M., Roberts-Thomson R., Brady B., Kefford R., Haydon A. et al. Optimizing combination dabrafenib and trametinib therapy in BRAF mutation-positive advanced melanoma patients: Guidelines from Australian melanoma medical oncologists. Asia-Pac. J. Clin. Oncol. 2016;12:5—12. doi: 10.1111/ajco.12656
- Инструкция по медицинскому применению препарата Тафинлар.
- Инструкция по медицинскому применению препарата Мекинист.
694136/ONCO/DIG/08.23/0




