Анти-VEGF-терапия — это патогенетическое лечение, которое способствует регрессии неоваскуляризации при пролиферативной диабетической ретинопатии (ПДР) и диабетическом макулярном отеке (ДМО) за счет воздействия на общую патогенетическую причину — фактор роста эндотелия сосудов — Vascular Endothelial Growth Factor (VEGF). Эффективность такого подхода подтверждена рядом крупных клинических исследований, в числе которых PROTOCOL S и PRIDE1–3.
PROTOCOL S
Основные элементы исследования
Проспективное многоцентровое рандомизированное исследование III фазы PROTOCOL S посвящено оценке эффективности и безопасности терапии ранибизумабом в дозе 0,5 мг в сравнении с панретинальной лазеркоагуляцией (ПРЛК) у пациентов с ПДР1,2. Динамика тяжести заболевания оценивалась по фотографиям глазного дна с использованием шкалы оценки тяжести диабетической ретинопатии (ДР) — Diabetic Retinopathy Severity Scale scores (DRSS).
Основные элементы исследования представлены на рис. 1.
Цель: оценить эффективность и безопасность интравитреальных инъекций ранибизумаба vs ПРЛК у пациентов с ПДР1,2.
Группа пациентов, включенных в исследование
394 пациента с ПДР с или без ДМО
Первичная конечная точка
Среднее изменение остроты зрения (ОЗ) через 5 лет терапии (изначально — 2 года)
Вторичные конечные точки:
-
потеря периферических полей зрения;
-
развитие угрожающего зрению ДМО;
-
офтальмологическая и системная безопасность.
Результаты и выводы
Результаты исследования подтвердили целесообразность терапии ПДР ранибизумабом или ПРЛК.
Рисунок 1. Основные элементы исследования PROTOCOL S
Результаты исследования за 2 года показали, что у 42,3% (n = 80) глаз при лечении ранибизумабом было зарегистрировано улучшение на 2 и более ступеней по шкале DRSS по сравнению с 23,1% (n = 46) глаз из группы ПРЛК. Такое же улучшение наблюдалось в группе ранибизумаба у 58,5% (n = 24) глаз с ДМО на исходном уровне и 37,8% (n = 56) глаз без ДМО. Ключевые данные эффективности — табл. 1.
Таблица 1 — Параметры улучшения ДР по шкале DRSS за 1 год
| Параметры улучшения/ухудшения | Ранибизумаб 0,5 мг (n = 189) | ПРЛК (n = 199) | Различия в доле (%), ДИ |
| Улучшение на ≥ 2 шага, n (%) | 79 (41,8) | 29 (14,6) | 27,4 (18,9; 35,9) |
| Улучшение на ≥ 3 шага, n (%) | 54 (28,6) | 6 (3,0) | 25,7 (18,9; 32,6) |
| Ухудшение на ≥ 2 шага, n (%) | 3 (1,6) | 23 (11,6) | -9,9 (-14,7; -5,2) |
| Ухудшение на ≥ 3 шага, n (%) | 1 (0,5) | 8 (4,0) | -3,4 (-6,3; -0,5) |
Эффективность ранибизумаба была достигнута уже к первому году лечения.
В дальнейшем для сохранения зрения пациентам требовалось около 3 инъекций в год (рис. 2). Через 5 лет у 42% пациентов тяжесть ДР снизилась на ≥ 2 шага по шкале DRSS по сравнению с 15% в группе ПРЛК. Безопасность лечения по частоте системных нежелательных явлений была сопоставима с ПРЛК.
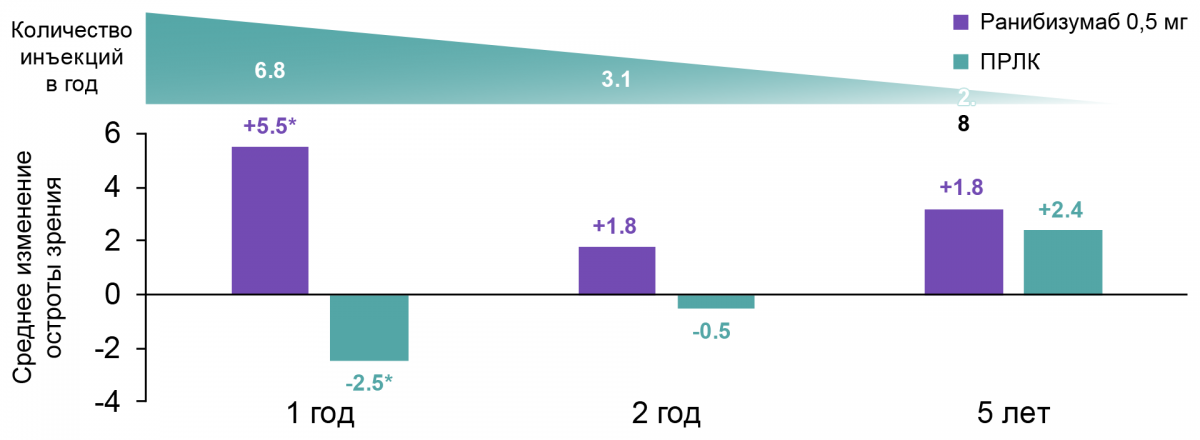
Рисунок 2. Изменение ОЗ и количества инъекций в течение 5 лет
Оценка эффективности и безопасности
-
Ранибизумаб обеспечивает бОльшую прибавку по ОЗ в результате терапии в течение 2 лет vs ПРЛК. Сопоставимое изменение ОЗ в группах ранибизумаб и ПРЛК через 5 лет.
-
Терапия ранибизумабом приводит к значительно меньшей потере полей зрения и меньшей вероятности витрэктомий vs ПРЛК.
-
Сопоставимая доля глаз без активной неоваскуляризации при лечении ранибизумабом ПРЛК.
-
Снижение тяжести ≥ 2 шага DRSS у 42% пациентов с ПДР через 5 лет терапии vs 15% в группе ПРЛК. После 1-го года терапии пациентам требуется ~ 3 инъекции в год для сохранения ОЗ.
-
Сопоставимые профили безопасности ранибизумаба и ПРЛК в течение 5 лет терапии.
PRIDE
Основные элементы исследования
Исследование PRIDE посвящено оценке эффективности и безопасности терапии ранибизумабом с или без ПРЛК по сравнению с монотерапией ПРЛК у пациентов с ПДР3. Основные элементы исследования представлены на рис. 3.
Цель: оценить эффективность и безопасность ранибизумаба с или без ПРЛК по сравнению с монотерапией ПРЛК у пациентов с ПДР.
Группа пациентов, включенных в исследование
106 пациентов с ПДР без ДМО
Первичная конечная точка
Изменения площади ретинальной неоваскуляризации
Результаты и выводы
В группе ранибизумаба наблюдался более сильный эффект на неоваскулярный ликедж при лучших исходах по ОЗ в сравнении с группой монотерапии ПРЛК
Рисунок 3. Основные элементы исследования PRIDE
Результаты исследования продемонстрировали, что ранибизумаб приводил к более выраженному уменьшению площади неоваскуляризации по сравнению с ПРЛК через 3 и 12 месяцев терапии. Значительное улучшение морфологических параметров было отмечено в группах ранибизумаба и комбинированной терапии на 3-м месяце (рис. 4)3.
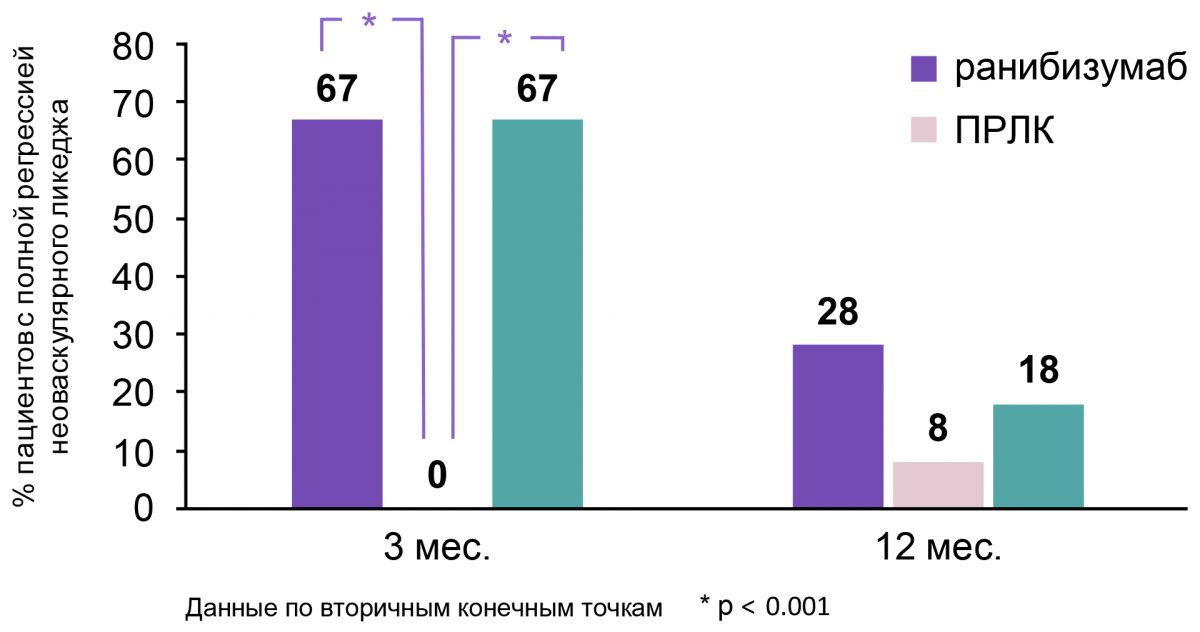
Рисунок 4. Динамика регрессии неоваскулярного ликеджа
В случае ПДР без ДМО ранибизумаб в большей степени снижал площадь неоваскуляризации и значительно улучшал исходы по ОЗ в сравнении с ПРЛК3.
Сравнение с другими клиническими исследованиями
Эффективность ранибизумаба в лечении ДР также подтверждена рядом крупных рандомизированных контролируемых исследований3,4 — рис. 5.
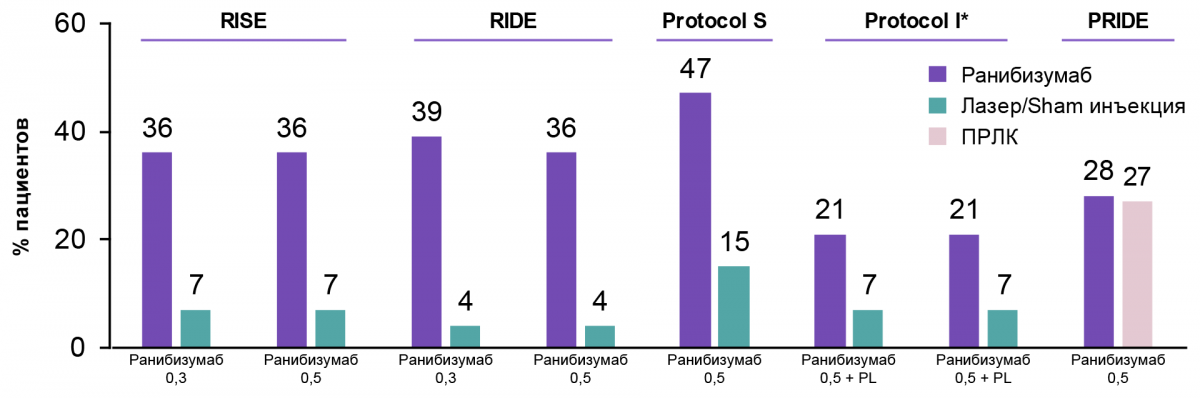
Данные не включают пациентов, у которых исходно не определялась тяжесть ДР.
Примечание.
* Объединенные данные ранибизумаб 0,5 + PL и ранибизумаб 0,5 + DL. Protocol I — результаты за 1 год.
Рисунок 5. Результаты клинических исследований, оценивавших эффективность ранибизумаба
Основные исследования эффективности и безопасности ранибизумаба: RIDE & RISE, Protocol S, Protocol I, RESTORE, REVEAL, REFINE, PRIDE1,5–11 показали, что в сравнении с плацебо ранибизумаб приводил к значительно большей вероятности улучшения ДР — на ≥ 2–3 шага по шкале DRSS от исходного уровня.
Источники:
- Gross JG, et al. JAMA. 2015; 314:2137–46.
- Gross JG, et al. JAMA Ophthalmol. doi:10.1001/jamaophthalmol.2018.3255.
- Lang, Gabriele E., et al. “Efficacy and Safety of Ranibizumabwith or without PanretinalLaser Photocoagulation versus Laser Photocoagulation Alone in Proliferative DiabeticRetinopathy –the PRIDE Study.” ActaOphthalmologica, 2019, pp. 1–10, doi:10.1111/aos.14312.
- David A Eichenbaum, et al. Data presented at American Academy of Optometry 2016.
- Nguy en QD, et al. Ophthalmology 2012; 119: 789–801.
- Brown DM, et al. Ophthalmology 2013; 120: 2013–22.
- Boyer et al. Ophthalmol 2015; 122: 2504–13. Michael S. et al., Ophthalmology 2017; 124: 596-603.
- Elman MJ, et al. Ophthalmology 2010; 117: 1064–77.
- Elman M, et al. Ophthalmology 2011; 118: 609–14.
- Elman M, et al. Ophthalmology 2012; 119: 2312–80.
- Bressler SB, et al. JAMA Ophthalmol. 2013; 131: 1033–40.
450574/VSI/WEB/052024/1
